题目内容
将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL 4.40mol/L盐酸中,充分反应后产生896mL H2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+.将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L.则原混合物中氧化铁的质量是( )
| A、2.4g | B、3.36g |
| C、5.60g | D、6.4g |
考点:有关混合物反应的计算
专题:计算题
分析:反应后溶液中还有较多H+离子剩余,且滤液中没有Cu2+,可知残留物没有Fe,只有Cu,而Cu可以残留说明溶液中没有Fe3+,溶液中阳离子为H+和Fe2+,参加反应的HCl中的H元素转化到氢气、水中,根据H原子守恒,计算混合物中O原子物质的量,根据Cu元素守恒计算n(CuO),再根据O原子守恒计算n(Fe2O3),根据m=nM计算氧化铁的质量.
解答:
解:反应后溶液中还有较多H+离子剩余,且滤液中没有Cu2+,可知残留物没有Fe,只有Cu,而Cu可以残留说明溶液中没有Fe3+,溶液中阳离子为H+和Fe2+,
反应后剩余n(H+)=0.4mol/L×0.2L=0.08mol,原溶液中n(HCl)=4.4mol/L×0.1L=0.44mol,
参加反应的HCl中的H元素转化到氢气、水中,根据H原子守恒,2n(H2O)+2n(H2)=n总(HCl)-n余(H+),即2n(H2O)+2×
=0.44mol-0.08mol,n(H2O)=0.14mol,故混合物中n(O)=n(H2O)=0.14mol,
由铜元素守恒,则n(CuO)=n(Cu)=
=0.02mol,
由O原子守恒:3n(Fe2O3)+n(CuO)=0.14mol,则n(Fe2O3)=0.04mol
m(Fe2O3)=0.04mol×160g/mol=6.4g,
故选D.
反应后剩余n(H+)=0.4mol/L×0.2L=0.08mol,原溶液中n(HCl)=4.4mol/L×0.1L=0.44mol,
参加反应的HCl中的H元素转化到氢气、水中,根据H原子守恒,2n(H2O)+2n(H2)=n总(HCl)-n余(H+),即2n(H2O)+2×
| 0.896L |
| 22.4L/mol |
由铜元素守恒,则n(CuO)=n(Cu)=
| 1.28g |
| 64g/mol |
由O原子守恒:3n(Fe2O3)+n(CuO)=0.14mol,则n(Fe2O3)=0.04mol
m(Fe2O3)=0.04mol×160g/mol=6.4g,
故选D.
点评:本题考查混合物计算,注意从溶液存在的离子判断物质反应的程度,注意利用守恒的方法计算,题目难度中等.

练习册系列答案
相关题目
下列溶液中各微粒的浓度关系一定正确的是( )
| A、某酸性溶液中只含NH4+、Cl-、H+、OH-四种离子,溶液中一定存在:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B、物质的量浓度相同的4种溶液:①CH3COONa;②NaNO3;③Na2CO3;④NaOH,pH的大小顺序是:④>③>①>② |
| C、在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| D、25℃时,pH=10的CH3COONa溶液与pH=10的氨水中,由水电离出的c(OH-)之比为1:1 |
下列叙述正确的是( )
| A、0.1mol/L NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) |
B、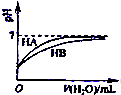 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液PH随加水量的变化,则NaA溶液的PH大于同浓度的NaB溶液的PH |
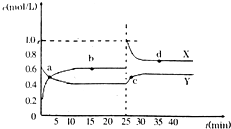
C、 表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是放热反应 |
D、 表示将1.000 mol/L氨水滴入20.00mL1.000 mol/L盐酸中,溶液PH和温度随加入氨水体积变化曲线 |
某无色溶液中只可能含有①Na+、②Ba2+、③Cl一、④I一、⑤SO32一、⑥SO42一 离子中的若干种(忽略水电离出的H+、OH一),依次进行下列实验,且每步所加试剂均过量,观察到现象如下表.下列结论正确的是( )
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈紫红色 |
| ③ | 向所得水溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A、肯定含有的离子是③④⑤ |
| B、肯定没有的离子是②⑤ |
| C、不能确定的离子是③⑥ |
| D、可能含有的离子是①⑥ |
下列关于常见有机物的说法中,不正确的是( )
| A、甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| B、乙烯使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的反应类型不同 |
| C、塑料、合成橡胶、合成纤维都属于合成有机高分子材料 |
| D、化学式均为(C6H10O5)n的淀粉和纤维素互为同分异构体 |
X、Y、Z、W是原子序数依次递增的四种短周期元素,甲、乙、丙、丁是它们两两组合而形成的化合物,且能发生反应:甲+乙→丙+丁,乙、丙、丁的化学式分别为Y2Z、YW2、ZX4,丁是一种常见的液体溶剂,0.1mol/L甲的水溶液的pH为1(25℃).下列说法正确的是( )
| A、原子半径:W>Z>Y>X |
| B、Z元素在周期表的位置为第三周期第ⅡA族 |
| C、丁的稳定性小于甲烷 |
| D、丙的水溶液呈碱性 |
 有关元素A、B、C、D的信息如下:
有关元素A、B、C、D的信息如下: 一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的卤代烃的种类共有( )
一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的卤代烃的种类共有( )