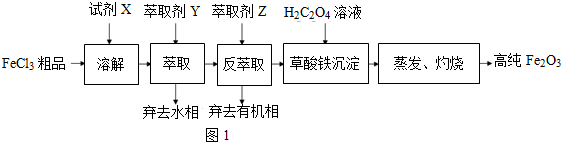
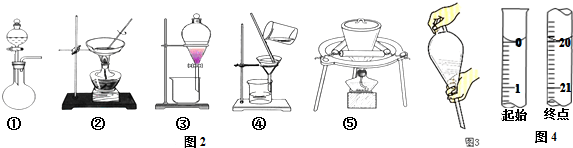
��Ŀ����
15���л�������PMMA�����ԡ�����ϩ�������MMA����Ϊ���壬ͨ���Ӿ۷�Ӧ�õ���ij����С�����ñ�ͪΪ��Ҫԭ��ͨ������;���ϳ�PMMA��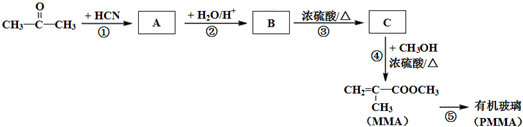
��֪��
 $\stackrel{+HCN}{��}$
$\stackrel{+HCN}{��}$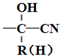
��ش��������⣺
��1��C�к��������ŵ��������Ȼ�������ٵķ�Ӧ�����Ǽӳɷ�Ӧ��
��2��B�Ľṹ��ʽ
 ��
����3��C��MMA�Ļ�ѧ����ʽ
 ��
����4�������ĸ��������У��뻯����MMA���еĹ�������ͬ���һ�Ϊͬ���칹����AD��
A��
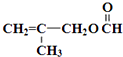
B��
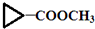
C��
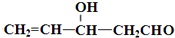
D��CH3COOCH=CH-CH3
��5����ƴӡ���ȩ��CH3CHO���������ᣨ
 �����ĺϳ�·�ߣ��Լ����ܼ���ѡ���ϳ�·�߲��ա���֪���е���д��ʽ��
�����ĺϳ�·�ߣ��Լ����ܼ���ѡ���ϳ�·�߲��ա���֪���е���д��ʽ�� ��
��
���� C��״�����������Ӧ���� ����֪CΪ
����֪CΪ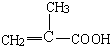 ������Ŀ��Ϣ��֪����ͪ��HCN�����ӳɷ�Ӧ����AΪ
������Ŀ��Ϣ��֪����ͪ��HCN�����ӳɷ�Ӧ����AΪ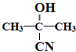 �����ת����ϵ��֪Aˮ������BΪ
�����ת����ϵ��֪Aˮ������BΪ ��B������ȥ��Ӧ����C��
��B������ȥ��Ӧ����C�� �����Ӿ۷�Ӧ�õ�PMMAΪ
�����Ӿ۷�Ӧ�õ�PMMAΪ ��
��
��� �⣺C��״�����������Ӧ���� ����֪CΪ
����֪CΪ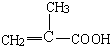 ������Ŀ��Ϣ��֪����ͪ��HCN�����ӳɷ�Ӧ����AΪ
������Ŀ��Ϣ��֪����ͪ��HCN�����ӳɷ�Ӧ����AΪ �����ת����ϵ��֪Aˮ������BΪ
�����ת����ϵ��֪Aˮ������BΪ ��B������ȥ��Ӧ����C��
��B������ȥ��Ӧ����C�� �����Ӿ۷�Ӧ�õ�PMMAΪ
�����Ӿ۷�Ӧ�õ�PMMAΪ ��
��
��1��CΪ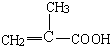 ��C�к��������ŵ��������Ȼ�������ٵķ�Ӧ�����Ǽӳɷ�Ӧ��
��C�к��������ŵ��������Ȼ�������ٵķ�Ӧ�����Ǽӳɷ�Ӧ��
�ʴ�Ϊ���Ȼ����ӳɷ�Ӧ��
��2��B�Ľṹ��ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��3��C��MMA�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4���뻯����MMA���еĹ�������ͬ������̼̼˫�����������һ�Ϊͬ���칹����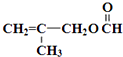 ��CH3COOCH=CH-CH3���������ֺ��й����Ų���ȫ��ͬ��
��CH3COOCH=CH-CH3���������ֺ��й����Ų���ȫ��ͬ��
�ʴ�Ϊ��AD��
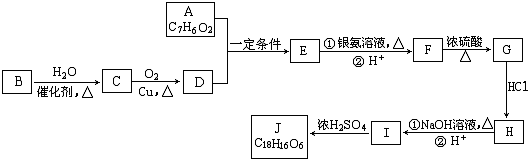
��5���ӡ���ȩ��CH3CHO���������ᣨ  �����ĺϳ�·������ͼΪ��
�����ĺϳ�·������ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶ���ϳɣ�ע����ݷ�Ӧ����������ϩ������Ľṹ�����ƶϣ��������չ����ŵ�������ת���ǹؼ����Ѷ��еȣ�

��ϰ��ϵ�д�
 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д�
�����Ŀ
3������˵������ȷ���ǣ�������
| A�� | �������ͳ�Ʒ����������о���ʵ�鷽����ģ�ͻ��������ǻ�ѧ�о��ij��÷��� | |
| B�� | ����������������ֹ����ȡ��������ͭ��ú��������ȡ���ȹ��̶��漰��ѧ�仯 | |
| C�� | ��2016��1��1�ſ�ʼ�㽭ʡ���ͱ��ɡ���������ߵ�����V�������Ⲣ����ζ�����������ŷŵ������� | |
| D�� | ��������������Ƽ����ķ�չ����ʹ���Ӿ���ܡ�����оƬ�����ӵ��ߡ����Ӽ�����Ȼ�ѧ�����õ��㷺��Ӧ�� |
20��Ĥ����ԭ���ڻ������������Ź㷺��Ӧ�ã������������õ绯ѧԭ���Ʊ������������ɫ������N2O5��װ��ͼ���£�����˵������ȷ���ǣ�������
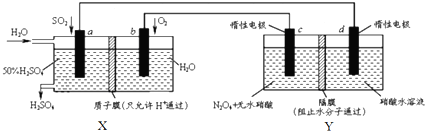

| A�� | X��ԭ��أ��ܹ��������ᣮY�ǵ��أ��ܹ�����N2O5 | |
| B�� | c�缫�ĵ缫��Ӧ����ʽΪ��N2O4+2HNO3-2e-=2N2O5+2H+ | |
| C�� | ����·��ͨ��2mol e-��X��Y�и���1molH+�����Ǩ�Ƶ��ұ� | |
| D�� | Ϊ��֤X������������������䣬������n��so2����n��H2O��=1��7.4 |
7������ʵ�����������ͽ��۾���ȷ���ǣ�������
| ѡ�� | ʵ����� | ʵ������ | ���� |
| A | ��Ũ��ˮ�ӵ�ʢ��AgCl������Թ��� | AgCl������ȫ�ܽ� | ������Һ��c��Ag+��•c��Cl-�� ��Ksp��AgCl�� |
| B | ��FeI2��Һ��ͨ������������������Ӧ�����Һ�еμ�KSCN��Һ | ��Һ��Ϊ��ɫ | Cl2�ܽ�Fe2+������Fe3+ |
| C | ����崿���еμ�����Ũ���ᣬ������������ͨ�뱽������Һ | ��Һ����� | ���ԣ����̼����� |
| D | �����ݵ�������Һ�зֱ�μӱ���NaCl��Һ��CuSO4��Һ | ���й������� | �����ʾ��������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
4��������X�ϳ���ϩ�Ʒ�Y��һ��·�����£�
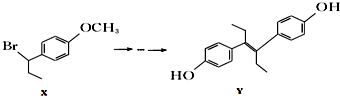
����������ȷ���ǣ�������

����������ȷ���ǣ�������
| A�� | ������x�в���������̼ԭ�� | |
| B�� | 1mol������Y��Ũ��ˮ��Ӧ���������5mol Br2 | |
| C�� | ��һ�������»�����Y�ܷ����Ӿ۷�Ӧ�����۷�Ӧ | |
| D�� | ����������ˮ��Һ�м��ȣ�������X�ܷ�����ȥ��Ӧ |
14�������ѣ�Ti��������Խ������Ϊ�����������������ҵ������������Ҫ�ɷ�FeTiO3����FeO��Al2O3��SiO2�����ʣ�Ϊ��Ҫԭ��ұ�������ѣ��������Ĺ�������ͼ��ͼ��
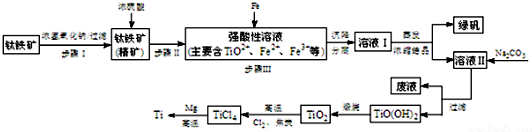
��֪����2H2SO4��Ũ��+FeTiO3=TiOSO4+FeSO4+2H2O
��TiO2+��ˮ�⣬ֻ�ܴ�����ǿ������Һ�У�
��1������I�з�����Ӧ�����ӷ���ʽ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O��
��2��25��ʱ�����ܵ�����γɳ�����pH��ϵ���
TiO��OH��2�ܶȻ�Ksp=1��10-29
a������II������мԭ���ǽ�Fe3+ת��ΪFe2+����ֹFe3+��TiO2+ͬʱ���ɳ�����
b������ҺII�м���Na2CO3��ĩ�������ǵ���PH������TiO��OH��2��Һ����Һ���д������е���������TiO2+��Fe2+��H+��
��3��TiCl4��Ti��Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ����������ķ�������õ�Ti��
��д����TiO2��ȡTiCl4�Ļ�ѧ����ʽTiO2+2Cl2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO��
�����������Ϣ������ȵ��¶��Ը���1412�漴�ɣ�
��4��Ϊ�˲ⶨ�̷���FeSO4•7H2O���ĺ�������ȡ2.850g�̷���Ʒ���ó�250mL��Һ��ȡ25.00mL��0.01mol/L����KMnO4��Һ���еζ���5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��������KMnO4��Һ�����Ϊ20mL����������Ʒ��FeSO4•7H2O����������Ϊ97.5%��

��֪����2H2SO4��Ũ��+FeTiO3=TiOSO4+FeSO4+2H2O
��TiO2+��ˮ�⣬ֻ�ܴ�����ǿ������Һ�У�
��1������I�з�����Ӧ�����ӷ���ʽ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O��
��2��25��ʱ�����ܵ�����γɳ�����pH��ϵ���
| pH | Fe��OH��3 | Fe��OH��2 | Mg��OH��2 | Ti��OH��2 |
| ��ʼ���� | 1.1 | 4.5 | 7 | 1 |
| ��ȫ���� | 2.8 | 6.4 | 9.2 | 2.7 |
a������II������мԭ���ǽ�Fe3+ת��ΪFe2+����ֹFe3+��TiO2+ͬʱ���ɳ�����
b������ҺII�м���Na2CO3��ĩ�������ǵ���PH������TiO��OH��2��Һ����Һ���д������е���������TiO2+��Fe2+��H+��
��3��TiCl4��Ti��Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ����������ķ�������õ�Ti��
��д����TiO2��ȡTiCl4�Ļ�ѧ����ʽTiO2+2Cl2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO��
�����������Ϣ������ȵ��¶��Ը���1412�漴�ɣ�
| TiCl4 | Mg | MgCl2 | Ti | |
| �۵�/�� | -25.0 | 648.8 | 714 | 1667 |
| �е�/�� | 136.4 | 1090 | 1412 | 3287 |

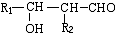
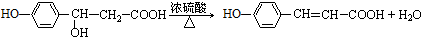 ��
��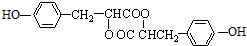 ��
��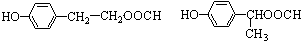 ��
��