题目内容
短周期主族元素A、B、C、D的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,B位于第VA族,A和C同主族,D原子最外层电子数与电子层数相等.下列叙述正确的是( )
| A、原子半径:D>C>B |
| B、单质的还原性:D>C |
| C、元素A、B、C的氧化物均为共价化合物 |
| D、元素B、C、D的最高价氧化物对应的水化物能相互反应 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期主族元素A、B、C、D的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,B位于第VA族,该化合物为氨气,可推知A为氢元素、B为N元素;A和C同主族,C的原子序数大于N,则C为Na;D原子序数大于Na,处于第三周期,D原子最外层电子数与电子层数相等,则D为Al,结合元素周期律与元素化合物性质解答.
解答:
解:短周期主族元素A、B、C、D的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,B位于第VA族,该化合物为氨气,可推知A为氢元素、B为N元素;A和C同主族,C的原子序数大于N,则C为Na;D原子序数大于Na,处于第三周期,D原子最外层电子数与电子层数相等,则D为Al,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>N,故A错误;
B.金属性Na>Al,故还原性Na>Al,故B错误;
C.H元素、N元素的氧化物均为共价化合物,Na的氧化物属于离子化合物,故C错误;
D.氢氧化铝是两性氢氧化物,能与硝酸、氢氧化钠反应,硝酸与氢氧化钠发生中和反应,故D正确,
故选D.
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>N,故A错误;
B.金属性Na>Al,故还原性Na>Al,故B错误;
C.H元素、N元素的氧化物均为共价化合物,Na的氧化物属于离子化合物,故C错误;
D.氢氧化铝是两性氢氧化物,能与硝酸、氢氧化钠反应,硝酸与氢氧化钠发生中和反应,故D正确,
故选D.
点评:本题考查结构性质位置关系应用,推断元素种类是关键,侧重对元素周期律的考查,难度不大.

练习册系列答案
相关题目
有四位学生分别设计了以下实验方案,并都认为如果观察到的现象和自己设计的方案一致,即可得出相应结论,你认为合理且正确的是( )
A、试液
| ||||||||
B、试液
| ||||||||
C、试液
| ||||||||
D、试液
|
室温,把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混合,则混合液中微粒浓度关系正确的为( )
| A、c (CH3COO-)>c (Na+) |
| B、c (OH-)>c (H+) |
| C、c (CH3COOH)>c (CH3COO-) |
| D、c (CH3COOH)+c (CH3COO-)=0.02mol/L |
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物的熔点较高 |
| D、XW2分子中各原子最外层电子均达到8电子结构 |
将一小块钠投入盛有硫酸铜溶液的烧杯中,不可能观察到的现象是( )
| A、钠熔成小球并在液面上游动 |
| B、有气体生成 |
| C、溶液底部析出红色物质 |
| D、溶液颜色变浅且有蓝色沉淀生成 |
下列物质中分子内和分子间均可形成氢键的是( )
| A、NH3 |
B、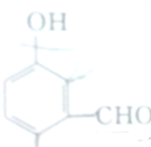 |
| C、H2S |
| D、C2H5OH |

 +CH3COOH→
+CH3COOH→ 聚合物
聚合物 可用于制备高吸水性树脂,其单体的结构简式为
可用于制备高吸水性树脂,其单体的结构简式为