题目内容
将一小块钠投入盛有硫酸铜溶液的烧杯中,不可能观察到的现象是( )
| A、钠熔成小球并在液面上游动 |
| B、有气体生成 |
| C、溶液底部析出红色物质 |
| D、溶液颜色变浅且有蓝色沉淀生成 |
考点:钠的化学性质
专题:元素及其化合物
分析:Na的密度小于水,熔点较低,Na先与溶液中的H2O剧烈反应生成H2和NaOH,且同时放出大量热,NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,据此分析解答.
解答:
解:Na的密度小于水,熔点较低,Na先与溶液中的H2O剧烈反应生成H2和NaOH,且同时放出大量热,放出的热量使钠熔成小球,钠受力不均导致其四处游动,生成的NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,
A.通过以上分析知,钠熔成小球并在液面上游动,故A不选;
B.钠和水反应生成氢气,所以有气体生成,故B不选;
C.NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,所以Na不会置换出Cu,故C选;
D.NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,溶液中铜离子浓度降低,所以溶液颜色变浅且有蓝色沉淀生成,故D不选;
故选C.
A.通过以上分析知,钠熔成小球并在液面上游动,故A不选;
B.钠和水反应生成氢气,所以有气体生成,故B不选;
C.NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,所以Na不会置换出Cu,故C选;
D.NaOH再与CuSO4反应生成Cu(OH)2蓝色沉淀,溶液中铜离子浓度降低,所以溶液颜色变浅且有蓝色沉淀生成,故D不选;
故选C.
点评:本题考查钠的性质,侧重考查元素化合物知识,明确反应先后顺序是解本题关键,注意在金属活动性顺序表中K、Ca、Na不能置换出其后面金属盐溶液中的金属单质,为易错点.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
化学物A的结构简式是HO-CH2-CBr2-O-CBr2-CH2-OH,下列有关A的叙述正确的是( )
| A、不能发生消去反应 |
| B、能发生取代反应 |
| C、能溶于水 |
| D、不能氧化为醛 |
X、Y、Z三种元素的原子,其最外层电子排布为ns1,3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
| A、X3YZ3 |
| B、X2YZ2 |
| C、XYZ2 |
| D、XYZ3 |
24mL 0.05mol/L的Na2SO3溶滚,恰好与20mL0.02mol/L的K2Cr2O7溶液完全反应,亚硫酸钠被氧化为Na2SO4,则铬元素在还原产物中的化合价为( )
| A、+6 | B、+3 | C、+2 | D、0 |
短周期主族元素A、B、C、D的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,B位于第VA族,A和C同主族,D原子最外层电子数与电子层数相等.下列叙述正确的是( )
| A、原子半径:D>C>B |
| B、单质的还原性:D>C |
| C、元素A、B、C的氧化物均为共价化合物 |
| D、元素B、C、D的最高价氧化物对应的水化物能相互反应 |
下列事实能用电化学原理解释的是( )
| A、银质物品久置表面变暗 |
| B、远洋海轮的尾部装上一定数量的锌板 |
| C、常温条件下,在空气中铝不易被腐蚀 |
| D、用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
下列说法中正确的是( )
| A、共价化合物中一定只含有极性共价键 |
| B、只含有共价键的物质一定是共价化合物 |
| C、离子化合物中可能含有极性共价键或非极性共价键 |
| D、有较强共价键存在的物质熔沸点一定很高 |

 和
和 为原料制备
为原料制备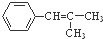 的合成路线流程图(无机试剂任用).合成路线流程图示例如图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如图: