题目内容
7.(1)请写出烷烃CnH${\;}_{2n+{2}_{\;}}$(n≥1)在足量的氧气中充分燃烧的化学方程式:2CnH2n+2+(3n+1)O2$\stackrel{点燃}{→}$2nCO2+(2n+2)H2O.有①甲烷,②乙烷,③丙烷,④丁烷4种烷烃,试回答(2)~(4)题(填序号):
(2)相同状况下,等体积的上述气态烃充分燃烧,消耗O2的量最多的是④.
(3)等质量的上述气态烃,在充分燃烧时,消耗O2的量最多的是①.
(4)10mL某气态烃,在50mL02中充分燃烧,得到液态水,以及体积为35mL的混合气体(所有气体体积均在同温、同压下测定).该气态烃是乙烷.
分析 (1)在空气中充分燃烧生成二氧化碳和水,根据原子守恒配平方程式;
(2)相同状况下,等体积的气态烃,消耗O2的量取决于(x+$\frac{y}{4}$)的值,(x+$\frac{y}{4}$)越大消耗O2的量越多;
(3)等质量的烃,在充分燃烧时,消耗O2的量取决于H的质量分数ω(H),ω(H)越大消耗O2的量越多;
(4)根据完全燃烧消耗O2的量,先判断是否完全燃烧,再根据方程式利用差量法计算.
解答 解:(1)烷烃CnH${\;}_{2n+{2}_{\;}}$(n≥1)在足量的氧气中充分燃烧生成二氧化碳和水,反应的化学方程式为2CnH2n+2+(3n+1)O2$\stackrel{点燃}{→}$2nCO2+(2n+2)H2O.
故答案为:2CnH2n+2+(3n+1)O2$\stackrel{点燃}{→}$2nCO2+(2n+2)H2O;
(2)①甲烷,分子式为CH4②乙烷,分子式为C2H6③丙烷,分子式为C3H8,④丁烷,分子式为C4H10,它们的(x+$\frac{y}{4}$)值分别为2、3.5、5、6.5,丁烷的(x+$\frac{y}{4}$)值最大,即消耗O2的量最多,
故答案为:④;
(3)①甲烷,分子式为CH4②C、H原子个数比为1:4,H的质量分数ω(H)最大,消耗O2的量最多,
故答案为:①;
(4)①甲烷,②乙烷,③丙烷,④丁烷4种烷烃中它们的(x+$\frac{y}{4}$)值分别为2、3.5、5、6.5,10ml完全燃烧需要的氧气的体积分别为20ml、35ml、50ml、65ml,
所以只有丁烷不能完全燃烧,
若完全燃烧,则混合气体是CO2、O2,设烃为CxHy,则
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(l),体积减小△V
1 1+(x+$\frac{y}{4}$)-x=1+$\frac{y}{4}$
10 (10+50-35)=25
所以10(1+$\frac{y}{4}$)=25,解得y=6,即1分子烃中H的原子个数是6,
氧气有剩余,所以10(x+$\frac{y}{4}$)<50,由于y=6,解得x<3.5,
所以气态烃为乙烷,
若不完全燃烧,10mL丁烷生成CO需要氧气为45ml,小于50ml,所以混合气体是CO2、CO,设烃为CxHy,根据C原子守恒,有10x=35,解得,x=3.5,碳原子数目为整数,不成立.
故答案为:乙烷.
点评 本题是一道有关有机物计算的题目,考查学生分析、解决问题的能力和计算能力,难度中等,熟记结论,使用体积差的计算方法要注意.

| A. | 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 | |
| B. | 向FeCl2溶液中滴加氯水,溶液颜色变为棕黄色,说明氯水中含有HClO | |
| C. | 向氯水中滴加稀硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| D. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
①单位时间内生成n molO2的同时生成2n molNO2
②用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1
③混合气体的颜色不再改变
④混合气体的密度不再改变
⑤混合气体的平均相对分子质量不再改变.
| A. | ①③⑤ | B. | ①④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
| A. | N2的消耗量是3.0mol | |
| B. | N2的平均速率是0.5mol•(L•min)-1 | |
| C. | N2的平衡浓度是1.0mol•L-1 | |
| D. | N2反应的量占原物质的量的百分数是50% |
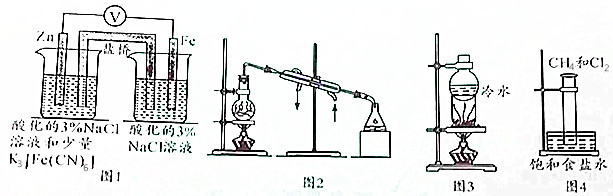
| A. | 用图1所示装置验证牺牲阳极的阴极保护法 | |
| B. | 用图2所示装置可在实验室制备蒸馏水 | |
| C. | 用图3所示装置可以进行NaCl与NH4Cl、NaCl与I2的分离 | |
| D. | 用图4所示装置进行CH4取代反应的实验 |
| A. | 分子中3个碳原子在同一直线上 | B. | 分子中所有原子在同一平面上 | ||
| C. | 与HCl加成只生成一种产物 | D. | 能与Cl2发生加成反应 |
(一)鉴别NaCl和NaNO2
甲同学用沉淀分析法
经查:常温下Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10.分别向盛有5mL 0.0001 mol/L两种盐溶液的试合中同时逐滴滴加0.0001mol•L-1硝酸银溶液,先生成沉淀的是装有NaCl溶液的试管.
乙同学侧定溶液pH
用pH试纸分别测定0.1 mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.该溶液呈碱性的原因是NO2-+H2O?HNO2+OH-(用离子方程式解释).
(二)该小组用如下装置(略去夹持仪器)制备亚硝酸钠

已知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO和NO2都能与MnO4一反应生成NO3一和Mn2+•
(1)使用铜丝的优点是可以控制反应的发生与停止.
(2)装置A中反应方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
装置C 中盛放的药品是C;(填字母代号)
A.浓硫酸 B.NaOH 溶液 C.水 D.四氯化碳
仪器F的作用防止水蒸气进入.
(3)该小组称取5.000g制取的样品溶于水配成250.0 mL溶液,取25.00mL溶液于锥形
瓶中,用0.1000mol/L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.7 | 20.12 | 20.00 | 19.88 |
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O.
③该样品中亚硝酸钠的质量分数为69%.
 ,写出其同分异构体的结构简式:
,写出其同分异构体的结构简式: .
.