题目内容
ClO-、ClO2-、ClO3-、ClO4-中,Cl都是以sp3杂化轨道与O成键,则ClO-是 形,ClO2-是 形,ClO3-是 形,ClO4-是 形.
考点:判断简单分子或离子的构型
专题:化学键与晶体结构
分析:根据价层电子对互斥理论来确定其空间构型,价层电子对个数=σ键个数+孤电子对个数.
解答:
解:次氯酸根离子中只含一个氯原子和一个氧原子,所以是直线形;
ClO2-中价层电子对个数=2+
(7+1-2×2)=4,且含有2个孤电子对,所以是V形;
ClO3-中价层电子对个数=3+
(7+1-3×2)=4,且含有一个孤电子对,所以是三角锥形;
ClO4-中价层电子对个数=4+
(7+1-4×2)=4,且不含孤电子对,所以是正四面体形,
故答案为:直线;V;三角锥;正四面体.
ClO2-中价层电子对个数=2+
| 1 |
| 2 |
ClO3-中价层电子对个数=3+
| 1 |
| 2 |
ClO4-中价层电子对个数=4+
| 1 |
| 4 |
故答案为:直线;V;三角锥;正四面体.
点评:本题考查了微粒的空间构型,根据价层电子对互斥理论确定其空间构型,注意孤电子对的确定方法.

练习册系列答案
相关题目
在a L Fe2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-完全沉淀;若加入足量强碱并加热可得到c mol NH3,则原溶液中Fe3+的浓度(mol?L-1)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
稀释某弱酸HA溶液时,浓度增大的是( )
| A、HA |
| B、H+ |
| C、A- |
| D、OH- |
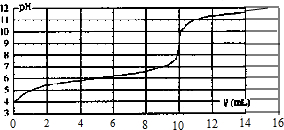 实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )
实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )| A、此一元弱酸HA的电离平衡常数Ka≈1×10-4mol?L-1 |
| B、此弱酸的起始浓度约为1×10-2mol?L-1 |
| C、此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂 |
| D、当混合液pH=7时,溶液中c(HA)>c(A-) |
海水是一个巨大的化学资源库,下列有关海水综合利用的说法错误的是( )
| A、海水中含有溴元素,需经过化学变化才可以得到溴单质 | ||||||||
| B、无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能 | ||||||||
| C、从海水中可以得到NaCl,电解熔融NaCl可制备金属钠 | ||||||||
D、从海水中提取镁可以采用下列方法:海水海水
|
现用pH=3的CH3COOH溶液和pH=11的NaOH溶液各V mL,进行中和滴定,当滴定到pH=7时,锥形瓶内溶液的体积为(滴定前后溶液未稀释、总体积不变)( )
| A、等于2V mL |
| B、小于2V mL |
| C、大于2V mL |
| D、无法确定 |