题目内容
海水是一个巨大的化学资源库,下列有关海水综合利用的说法错误的是( )
| A、海水中含有溴元素,需经过化学变化才可以得到溴单质 | ||||||||
| B、无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能 | ||||||||
| C、从海水中可以得到NaCl,电解熔融NaCl可制备金属钠 | ||||||||
D、从海水中提取镁可以采用下列方法:海水海水
|
考点:海水资源及其综合利用
专题:元素及其化合物
分析:A、海水中的溴元素需要通过氧化剂把溴离子氧化为溴单质,再利用还原剂还原溴单质为溴离子,通入氯气氧化为溴离子;
B、在波浪发电和潮汐发电过程中机械能转化为电能;
C、从海水中通过蒸发溶剂可以得到NaCl固体,电解熔融NaCl可制备金属钠;
D、海水提取镁的过程是先沉淀镁离子,价元素溶解生成氯化镁,蒸发结晶析出晶体,脱水的氯化镁;
B、在波浪发电和潮汐发电过程中机械能转化为电能;
C、从海水中通过蒸发溶剂可以得到NaCl固体,电解熔融NaCl可制备金属钠;
D、海水提取镁的过程是先沉淀镁离子,价元素溶解生成氯化镁,蒸发结晶析出晶体,脱水的氯化镁;
解答:
解:A、海水中的溴元素需要通过氧化剂把溴离子氧化为溴单质,再利用还原剂还原溴单质为溴离子,通入氯气氧化溴离子为溴单质;过程中 发生化学反应,故A正确;
B、在波浪发电和潮汐发电过程中机械能转化为电能,不是将化学能转化为电能,故B错误;
C、从海水中通过蒸发溶剂可以得到NaCl固体,电解熔融NaCl可制备金属钠是工业制备钠的方法,故C正确;
D、依据海水提取镁的原理分析,卤水中加入氢氧化钙沉淀镁离子生成氢氧化镁,过滤后加盐酸溶解后蒸发浓缩,冷却结晶析出晶体,在氯化氢气流中加热失去结晶水,得到氯化镁固体,电解熔融氯化镁得到镁金属,反应过程中需经过化学变化,故D正确;
故选B.
B、在波浪发电和潮汐发电过程中机械能转化为电能,不是将化学能转化为电能,故B错误;
C、从海水中通过蒸发溶剂可以得到NaCl固体,电解熔融NaCl可制备金属钠是工业制备钠的方法,故C正确;
D、依据海水提取镁的原理分析,卤水中加入氢氧化钙沉淀镁离子生成氢氧化镁,过滤后加盐酸溶解后蒸发浓缩,冷却结晶析出晶体,在氯化氢气流中加热失去结晶水,得到氯化镁固体,电解熔融氯化镁得到镁金属,反应过程中需经过化学变化,故D正确;
故选B.
点评:本题考查较为综合,为高频考点,侧重于学生的分析能力和知识的综合运用的考查,题目侧重化学与生活、生成的考查,有利于培养学生的良好科学素养、提高学习的聚集,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质中所含原子数与0.1molH3PO4所含原子数相等的是( )
| A、0.4molH2O |
| B、0.2molH2SO4 |
| C、0.4molHCl |
| D、0.3molHNO3 |
现有70g质量分数为70%的硫酸和50g含杂质20%的烧碱(杂质不参加反应),足量的铝屑.用上述原料生产Al(OH)3的量最多时消耗铝的质量为( )
| A、26g | B、36g |
| C、104g | D、130g |
已知相同温度下电离常数K(HF)>K(HCN),在物质的量浓度均为0.1mol/L的NaCN和NaF混合浓度中,下列排序正确的是( )
| A、c(OH-)>c(HF)>c(HCN)>c(H+) |
| B、c(OH-)>c(CN-)>c(F-)>c(H+) |
| C、c(OH-)>c(F-)>c(CN-)>c(H+) |
| D、c(F-)>c(OH-)>c(HCN)>c(HF) |
 同分异构体A1和A2分别与浓H2SO4在一定温度下共热都只生成烃B,B的蒸气密度是同温同压下H2密度的52倍,含碳的质量分数为92.3%.在催化剂存在下,1mol B可以和4mol H2发生加成反应.核磁共振氢谱显示,H有5个吸收峰.有关物质之间的转化关系如下:
同分异构体A1和A2分别与浓H2SO4在一定温度下共热都只生成烃B,B的蒸气密度是同温同压下H2密度的52倍,含碳的质量分数为92.3%.在催化剂存在下,1mol B可以和4mol H2发生加成反应.核磁共振氢谱显示,H有5个吸收峰.有关物质之间的转化关系如下:
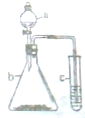 利用如图装置进行实验,仪器a、b、c中分别盛装下列试剂,试管c中现象描述正确的是( )
利用如图装置进行实验,仪器a、b、c中分别盛装下列试剂,试管c中现象描述正确的是( )