题目内容
 下图是元素周期表短周期中11种元素的化台价与原子序数的关系示意图,请回答下列问题(用具体的元素符号作答):
下图是元素周期表短周期中11种元素的化台价与原子序数的关系示意图,请回答下列问题(用具体的元素符号作答):(1)元素x、Y、z、W、R五种元素中属于金属元素的是
(2)由此图可以判断,11种元素中处于同主族的共有
(3)X、Y.Z三种元素的原子半径大小顺序为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)短周期元素,X化合价只有-2,可推知X为O元素,Y化合价为+1,原子序数大于O,故Y为Na,Z的化合价为+3,原子序数大于Na,Z为Al;W有+6、-2价,则W为S元素,R有+7、-1价,则R为Cl元素;
(2)由图可知,上述11种元素中,处于同主族的分别为ⅣA、ⅤA、ⅥA、ⅦA;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大;电子层结构相同,核电荷数越大离子半径越小.
(2)由图可知,上述11种元素中,处于同主族的分别为ⅣA、ⅤA、ⅥA、ⅦA;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大;电子层结构相同,核电荷数越大离子半径越小.
解答:
解:短周期元素,X化合价只有-2,可推知X为O元素,Y化合价为+1,原子序数大于O,故Y为Na,Z的化合价为+3,原子序数大于Na,Z为Al;W有+6、-2价,则W为S元素,R有+7、-1价,则R为Cl元素,
(1)上述五种元素中,Na、Al属于金属元素;Z的简单离子为Al3+,离子核外电子数为10,有2个电子层,各层电子数为2、8,离子结构示意图是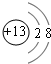 ,
,
故答案为:Na、Al; ;
;
(2)上述11种元素中,处于同主族的分别为ⅣA、ⅤA、ⅥA、ⅦA,共有4组,故答案为:4;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>Al>O;电子层结构相同,核电荷数越大离子半径越小,故离子半径O2->Na+>Al3+,故答案为:Na>Al>O;O2->Na+>Al3+.
(1)上述五种元素中,Na、Al属于金属元素;Z的简单离子为Al3+,离子核外电子数为10,有2个电子层,各层电子数为2、8,离子结构示意图是
 ,
,故答案为:Na、Al;
 ;
;(2)上述11种元素中,处于同主族的分别为ⅣA、ⅤA、ⅥA、ⅦA,共有4组,故答案为:4;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>Al>O;电子层结构相同,核电荷数越大离子半径越小,故离子半径O2->Na+>Al3+,故答案为:Na>Al>O;O2->Na+>Al3+.
点评:本题考查结构性质位置关系应用,根据化合价及原子序数确定元素是解题关键,注意掌握微粒半径比较.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
下列反应原理不符合工业冶炼金属实际情况的是( )
A、2HgO
| ||||
B、4Al+3MnO2
| ||||
C、2AlCl3
| ||||
D、4CO+Fe3O4
|
元素X和元素Y在周期表中位于相邻的两个周期:X与Y两原子核外电子总数之和为19;Y的原子核内质子数比X多3个.下列描述中不正确的是( )
| A、X与Y形成的化合物的化学式可能为Y2X2 |
| B、X的化合物种类比Y的化合物种类多 |
| C、Y能置换出酸中的氢,却不能置换出盐溶液中的金属 |
| D、X和Y都是性质很活泼的元素,在自然界中都只能以化合态形式存在 |
某二元酸(H2A)在水中的电离方程式为:H2A═H++HA- HA-?H++A2-(Ka=1.0×10-2),下列说法正确的是( )
| A、在0.1mol?L-1的H2A溶液中,c(H+)>0.12mol?L-1 |
| B、在0.1mol?L-1的Na2A溶液中,c(A2-)+c(HA-)+c(Na+)=0.2mol?L-1 |
| C、分别将同浓度(0.1mol?L-1)的NaHA和Na2A溶液等体积混合,其pH一定小于7 |
| D、0.1mol?L-1的NaHA溶液中离子浓度为:c(Na+)>c(H+)>c(HA-)>c(A2-)>c(OH-) |

 按如图装置进行实验,回答下列问题(C、C1、C2均为石墨电极).
按如图装置进行实验,回答下列问题(C、C1、C2均为石墨电极).
