题目内容
(1)根据下表左边的“实验操作”,从右边的“实验现象”中选择正确的字母代号,填入对应
“答案”的空格中.
(2)某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.
①提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成.
②设计实验:
ⅰ、利用右图装置分别对一定量的Na2CO3和NaHCO3进行加热;
ⅱ、为了检验CO2的生成,试管B中应加入的物质是 (填“澄清的石灰水”或“NaOH溶液”),检验CO2生成的化学方程式: .
③现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有 沉淀生成(填沉淀的颜色),说明Na2CO3和NaHCO3的热稳定性是:Na2CO3 NaHCO3(填“>”或“<”).
④某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为 L (标准状况).
“答案”的空格中.
| 实验操作 | 答案 | 实验现象 |
| ①让一束光线通过Fe(OH)3胶体 | A、呈蓝色 B、生成白色胶状沉淀 C、呈现光亮“通路” D、产生红褐色沉淀 | |
| ②向盛有FeCl3溶液的试管中加入NaOH溶液 | ||
| ③向Al2(SO4)3溶液中滴加氨水 | ||
| ④向土豆片上滴加碘水 |
①提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成.
②设计实验:

ⅰ、利用右图装置分别对一定量的Na2CO3和NaHCO3进行加热;
ⅱ、为了检验CO2的生成,试管B中应加入的物质是
③现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
④某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
考点:探究碳酸钠与碳酸氢钠的性质,化学实验方案的评价
专题:实验设计题
分析:(1)①胶体粒子的大小在1~100nm之间,具有丁达尔效应;
②向盛有FeCl3溶液的试管中加入NaOH溶液,反应生成Fe(OH)3红褐色沉淀;
③Al2(SO4)3可以和氨水之间反应生成氢氧化铝和硫酸铵;
④土豆中富含淀粉,碘单质遇到淀粉会变蓝色;
(2)②检验二氧化碳的常用试剂为澄清石灰水,二氧化碳与氢氧化钠溶液的反应没有明显现象;氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,据此写出反应的化学方程式;
③碳酸氢钠分解生成的二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀,说明碳酸氢钠的稳定性小于碳酸钠;
④根据反应关系式计算出生成的二氧化碳气体在标况下的体积.
②向盛有FeCl3溶液的试管中加入NaOH溶液,反应生成Fe(OH)3红褐色沉淀;
③Al2(SO4)3可以和氨水之间反应生成氢氧化铝和硫酸铵;
④土豆中富含淀粉,碘单质遇到淀粉会变蓝色;
(2)②检验二氧化碳的常用试剂为澄清石灰水,二氧化碳与氢氧化钠溶液的反应没有明显现象;氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,据此写出反应的化学方程式;
③碳酸氢钠分解生成的二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀,说明碳酸氢钠的稳定性小于碳酸钠;
④根据反应关系式计算出生成的二氧化碳气体在标况下的体积.
解答:
解:(1)①Fe(OH)3胶体具有丁达尔效应,用一束强光照射,从垂直于光线的传播方向观察,现象是呈现光亮“通路”,故答案为:C;
②向盛有FeCl3溶液的试管中加入NaOH溶液,发生复分解反应FeCl3+3NaOH=Fe(OH)3↓+3NaCl,现象是生成Fe(OH)3红褐色沉淀,故答案为:D;
③向Al2(SO4)3溶液中滴加氨水发生复分解反应,反应的化学方程式为:Al2(SO4)3+6NH3?H2O=2Al(OH)3↓+3(NH4)2SO4,现象是出现白色胶状沉淀,
故答案为:B;
④土豆中富含淀粉,向土豆片上滴加碘水,碘单质遇到淀粉会变蓝色,所以会看到变蓝,故答案为:A;
(2)②由于氢氧化钠溶液与二氧化碳的反应没有明显现象,所以无法检验是否有二氧化碳生成,检验二氧化碳气体的常用试剂为澄清石灰水,将二氧化碳气体通入澄清石灰水,澄清石灰水会变浑浊,反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O,
故答案为:澄清石灰水;Ca(OH)2+CO2=CaCO3↓+H2O;
③碳酸钠加热不分解,而碳酸氢钠加热分解生成二氧化碳气体,二氧化碳通入澄清石灰水后,溶液变浑浊,生成了白色沉淀碳酸钙,说明碳酸钠稳定性大于碳酸氢钠,
故答案为:白色;>;
④碳酸氢钠分解的关系式为:2NaHCO3~CO2,8.4gNaHCO3的物质的量为:
=0.1mol,完全分解可以生成0.05mol二氧化碳,标况下0.05mol二氧化碳的体积为:22.4L/mol×0.05mol=1.12L,
故答案为:1.12.
②向盛有FeCl3溶液的试管中加入NaOH溶液,发生复分解反应FeCl3+3NaOH=Fe(OH)3↓+3NaCl,现象是生成Fe(OH)3红褐色沉淀,故答案为:D;
③向Al2(SO4)3溶液中滴加氨水发生复分解反应,反应的化学方程式为:Al2(SO4)3+6NH3?H2O=2Al(OH)3↓+3(NH4)2SO4,现象是出现白色胶状沉淀,
故答案为:B;
④土豆中富含淀粉,向土豆片上滴加碘水,碘单质遇到淀粉会变蓝色,所以会看到变蓝,故答案为:A;
(2)②由于氢氧化钠溶液与二氧化碳的反应没有明显现象,所以无法检验是否有二氧化碳生成,检验二氧化碳气体的常用试剂为澄清石灰水,将二氧化碳气体通入澄清石灰水,澄清石灰水会变浑浊,反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O,
故答案为:澄清石灰水;Ca(OH)2+CO2=CaCO3↓+H2O;
③碳酸钠加热不分解,而碳酸氢钠加热分解生成二氧化碳气体,二氧化碳通入澄清石灰水后,溶液变浑浊,生成了白色沉淀碳酸钙,说明碳酸钠稳定性大于碳酸氢钠,
故答案为:白色;>;
④碳酸氢钠分解的关系式为:2NaHCO3~CO2,8.4gNaHCO3的物质的量为:
| 8.4g |
| 84g/mol |
故答案为:1.12.
点评:本题考查碳酸钠与碳酸氢钠的性质,题目难度中等,熟悉丁达尔效应、Fe(OH)3、Al2(SO4)3、淀粉的性质是解答关键,注意掌握碳酸钠、碳酸氢钠的热稳定性大小,能够根据反应方程式进行简单的化学计算.

练习册系列答案
相关题目
常温下,将盐酸和一元碱MOH溶液等体积混合(忽略体积变化),两种溶液的浓度和混合后所得溶液的pH如下表:
下列判断不正确的是( )
| 实验编号 | 盐酸的浓度/(mol/L) | MOH溶液的浓度/(mol/L) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | 0.2 | c1 | 7 |
| 丙 | 0.1 | 0.1 | 5 |
| A、甲组混合溶液中M+水解程度较丙组中大,且a<5 |
| B、甲组混合溶液中:c(Cl-)>c(M+)>c(H+)>c(OH-) |
| C、乙组混合溶液中:c(M+)+c(MOH)>0.1mol/L,且c1>0.2 |
| D、丙组混合溶液中:c(OH-)+c(MOH)=10-5mol/L |
下列溶液中各离子的浓度由大到小排列顺序正确的是( )
| A、CH3COONa溶液中 c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| C、Na2CO3溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、NaHS溶液中:c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+) |
古诗词是古人为我们留下的宝贵精神财富,下列诗句中不涉及氧化还原反应的是( )
| A、野火烧不尽,春风吹又生 |
| B、爆竹声中一岁除,春风送暖入屠苏 |
| C、粉身碎骨浑不怕,要留清白在人间 |
| D、春蚕到死丝方尽,蜡炬成灰泪始干 |
 如表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用回答下列问题:
如表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用回答下列问题:
 下图是元素周期表短周期中11种元素的化台价与原子序数的关系示意图,请回答下列问题(用具体的元素符号作答):
下图是元素周期表短周期中11种元素的化台价与原子序数的关系示意图,请回答下列问题(用具体的元素符号作答):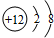 ,该离子的符号为
,该离子的符号为 1、欲用98%的浓硫酸(ρ=1.84g?cm-3)配制成浓度为0.25mol?L-1的稀硫酸500mL.
1、欲用98%的浓硫酸(ρ=1.84g?cm-3)配制成浓度为0.25mol?L-1的稀硫酸500mL.