题目内容
如图是一种常见的电化学装置.有关说法正确的是( )
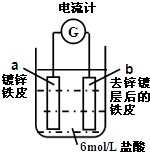

| A、a为阴极,铁皮受到保护 |
| B、盐酸中的Cl-向b定向移动 |
| C、在两个电极反应中,锌元素分别被氧化或被还原 |
| D、锌镀层完全溶解之时,电流计指针几乎没有偏转 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该原电池中,锌易失电子作负极、铁作正极,负极上电极反应式为Zn-2e-=Zn2+,正极上电极反应式为2H++2e-=H2↑,放电时,电解质溶液中阴离子向负极移动.
解答:
解:A.a电极锌易失电子作负极,作负极的金属加速被腐蚀,故A错误;
B.a为负极、b为正极,放电时,电解质溶液中氯离子向负极a移动,故B错误;
C.负极上锌失电子被氧化,正极上氢离子得电子 被还原,故C错误;
D.锌镀层完全溶解时,该装置不能构成原电池,则电流计指针几乎没有偏转,故D正确;
故选D.
B.a为负极、b为正极,放电时,电解质溶液中氯离子向负极a移动,故B错误;
C.负极上锌失电子被氧化,正极上氢离子得电子 被还原,故C错误;
D.锌镀层完全溶解时,该装置不能构成原电池,则电流计指针几乎没有偏转,故D正确;
故选D.
点评:本题考查了原电池原理,明确原电池正负极的判断方法、电极上发生的反应及离子移动方向即可解答,题目难度不大.

练习册系列答案
相关题目
常温下某H2CO3溶液的pH约为5.5,c(CO32-)约为5×10-11mol/L,该溶液中浓度最低的离子是( )
| A、HCO3- |
| B、CO32- |
| C、H+ |
| D、OH- |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L的H2O所含的分子数为NA |
| B、1mol T2O分子所含的中子数为10NA |
| C、常温常压下,20g D2O分子中所含的质子数为10NA |
| D、1mol H3O+所含的电子数为11NA |
吸进人体内的氧有2%转化为加速人体衰老的氧化性极强的活性氧,若Na2SeO3能清除人体内活性氧,则Na2SeO3的作用是( )
| A、还原剂 |
| B、氧化剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂又不是还原剂 |
下列化学用语中,表示正确的是( )
A、2s的电子云模型是: |
B、肽键的结构式为: |
C、H2S分子的球棍模型为: |
D、最外层电子排布式为ns2np3对应的轨道表示式为: |
设NA代表阿伏加德罗常数(NA)的数值,下列说法正确的是( )
| A、乙烯和环丙烷(C3H6)组成的28g混合气体中含有3NA个氢原子 |
| B、1mol碳酸钾晶体中含阴离子数为NA 个 |
| C、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
| D、将0.1mol氯化铁溶于1L水中,所得溶液中含有0.1NA Fe3+ |