题目内容
下列化学用语中,表示正确的是( )
A、2s的电子云模型是: |
B、肽键的结构式为: |
C、H2S分子的球棍模型为: |
D、最外层电子排布式为ns2np3对应的轨道表示式为: |
考点:结构式,球棍模型与比例模型,原子核外电子排布
专题:化学用语专题
分析:A.s电子云,是球形对称的;
B.肽键:一分子氨基酸的α-羧基和一分子氨基酸的α-氨基脱水缩合形成的酰胺键;
C.S原子的半径大于H原子的半径;
D.根据洪特规则进行判断.
B.肽键:一分子氨基酸的α-羧基和一分子氨基酸的α-氨基脱水缩合形成的酰胺键;
C.S原子的半径大于H原子的半径;
D.根据洪特规则进行判断.
解答:
解:A.s电子云,是球形对称的,在核外半径相同处任一方向上电子出现的几率相同,故A错误;
B.肽键:一分子氨基酸的α-羧基和一分子氨基酸的α-氨基脱水缩合形成的酰胺键,即-CO-NH-,其结构式为 ,故B正确;
,故B正确;
C.S原子的半径大于H原子的半径,故C错误;
D.根据洪特规则可知:分子分布到能量简并的原子轨道时,优先以自旋相同的方式分别占据不同的轨道,应为: ,故D错误,
,故D错误,
故选B.
B.肽键:一分子氨基酸的α-羧基和一分子氨基酸的α-氨基脱水缩合形成的酰胺键,即-CO-NH-,其结构式为
 ,故B正确;
,故B正确;C.S原子的半径大于H原子的半径,故C错误;
D.根据洪特规则可知:分子分布到能量简并的原子轨道时,优先以自旋相同的方式分别占据不同的轨道,应为:
 ,故D错误,
,故D错误,故选B.
点评:本题考查电子云、球棍模型、肽键的结构和等轨道表示式化学用语,为高频考点,题目难度不大.把握化学用语的规范应用是解答的关键.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、Na2CO3溶液的水解:CO32-+H3O+?HCO3-+H2O |
| B、钢铁吸氧腐蚀时,负极反应式为:4OH--4e-═2H2O+O2↑ |
| C、向Al2(SO4)3溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀:2Al3++3SO42-+8OH-+3Ba2+═2AlO2-+3BaSO4↓+4H2O |
| D、氯化亚铁溶液中滴入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
如图是一种常见的电化学装置.有关说法正确的是( )
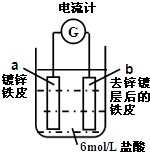

| A、a为阴极,铁皮受到保护 |
| B、盐酸中的Cl-向b定向移动 |
| C、在两个电极反应中,锌元素分别被氧化或被还原 |
| D、锌镀层完全溶解之时,电流计指针几乎没有偏转 |
将KClO3、I2各0.02mol加入12g 36.5%的盐酸中,I2恰好完全溶解,没有气体产生(不考虑盐酸的挥发).将反应后的溶液用冰水冷却,析出橙红色晶体A(A在常温下就有升华现象),过滤,将滤液蒸干,收集到KCl固体、8.7g液态水和极少量的A蒸气.则A的化学式可能是( )
| A、I2Cl6 |
| B、HClO |
| C、IClO |
| D、KIO3 |
下列叙述错误的是( )
| A、0.012kg12C中含有约6.02×1023个碳原子 |
| B、在同温同压下,1摩尔固体或液体的体积各不相同,1摩尔气体体积大约相等 |
| C、在使用摩尔表示物质的量的单位时,应指明粒子的种类 |
| D、只有在标准状况下,1摩尔气体积才约为22.4 L |
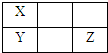 X、Y、Z、W均为短周期元素,原子序数依次增大,其中X、Y、Z在周期表中的相对位置如图所示.Y是短周期主族元素中原子半径最大的元素,W的最高正化合价与最低负化合价的代数和为0,下列说法中不正确的是( )
X、Y、Z、W均为短周期元素,原子序数依次增大,其中X、Y、Z在周期表中的相对位置如图所示.Y是短周期主族元素中原子半径最大的元素,W的最高正化合价与最低负化合价的代数和为0,下列说法中不正确的是( )| A、W的氧化物可以用于制造太阳能电池 |
| B、最高价氧化物对应水化物的碱性Y比X强 |
| C、可以用电解法制备Z单质 |
| D、Y和Z的最高价氧化物对应水化物之间可以相互反应 |
下列判断中一定正确的是( )
| A、若X、Y都是气态氢化物,且相对分子质量:X>Y,则沸点:X>Y |
| B、若X、Y属于同主族元素,且相对原子质量:X>Y,则X的失电子能力比Y强 |
| C、若R2-和M+的电子层结构相同,则原子序数:R>M |
| D、若M、N是同主族元素,且原子序数:M>N,则非金属性:M>N |
