题目内容
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L的H2O所含的分子数为NA |
| B、1mol T2O分子所含的中子数为10NA |
| C、常温常压下,20g D2O分子中所含的质子数为10NA |
| D、1mol H3O+所含的电子数为11NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
B.T2O分子中含有12个中子,1molT2O分子中含有12mol中子;
C.重水中含有10个质子,20g重水的物质的量为1mol,含有10mol质子;
D.水合氢离子含有10个电子,1mol中含有10mol电子.
B.T2O分子中含有12个中子,1molT2O分子中含有12mol中子;
C.重水中含有10个质子,20g重水的物质的量为1mol,含有10mol质子;
D.水合氢离子含有10个电子,1mol中含有10mol电子.
解答:
解:A.标况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故A错误;
B.1molT2O分子中含有12mol中子,所含的中子数为12NA,故B错误;
C.20g重水的物质的量为1mol,含有10mol质子,所含的质子数为10NA,故C正确;
D.1molH3O+所含的电子为10mol,含有的电子数为10NA,故D错误;
故选C.
B.1molT2O分子中含有12mol中子,所含的中子数为12NA,故B错误;
C.20g重水的物质的量为1mol,含有10mol质子,所含的质子数为10NA,故C正确;
D.1molH3O+所含的电子为10mol,含有的电子数为10NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标准状况下水不是气体,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
如图是印在食品包装内常见小袋子上的部分图案,该小袋子内的物质最有可能是( )


| A、铁粉 | B、氧化钠 |
| C、亚硫酸钠 | D、生石灰 |
下列表示对应化学反应的离子方程式正确的是( )
| A、Na2CO3溶液的水解:CO32-+H3O+?HCO3-+H2O |
| B、钢铁吸氧腐蚀时,负极反应式为:4OH--4e-═2H2O+O2↑ |
| C、向Al2(SO4)3溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀:2Al3++3SO42-+8OH-+3Ba2+═2AlO2-+3BaSO4↓+4H2O |
| D、氯化亚铁溶液中滴入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
下列反应能设计成原电池提供电能的是( )
| A、Cu与Cl2燃烧反应 |
| B、Ba(OH)2?8H2O与NH4Cl反应 |
| C、灼热的炭与CO2反应 |
| D、氢氧化钠溶液与稀盐酸反应 |
如图是一种常见的电化学装置.有关说法正确的是( )
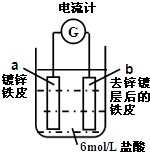

| A、a为阴极,铁皮受到保护 |
| B、盐酸中的Cl-向b定向移动 |
| C、在两个电极反应中,锌元素分别被氧化或被还原 |
| D、锌镀层完全溶解之时,电流计指针几乎没有偏转 |
下列叙述错误的是( )
| A、0.012kg12C中含有约6.02×1023个碳原子 |
| B、在同温同压下,1摩尔固体或液体的体积各不相同,1摩尔气体体积大约相等 |
| C、在使用摩尔表示物质的量的单位时,应指明粒子的种类 |
| D、只有在标准状况下,1摩尔气体积才约为22.4 L |

