��Ŀ����
12����һ������SO2��g����O2��g���ֱ�ͨ�����Ϊ2 L�ĺ����ܱ������У��ڲ�ͬ�¶��½��з�Ӧ���õ����±��е��������ݣ�������| ʵ�� ��� | �¶� /�� | ƽ�ⳣ�� /mol-1•L | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| SO2 | O2 | SO2 | O2 | ||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
| A�� | x=2.4 | |
| B�� | T1��T2�Ĺ�ϵ��T1��T2 | |
| C�� | K1��K2�Ĺ�ϵ��K2��K1 | |
| D�� | ʵ��1��ǰ6 min�ķ�Ӧ����v��SO2��=0.2 mol•L-1•min-1 |
���� ����ͼ�����ݣ����ݻ�ѧƽ������ʽ��ʽ����Ϸ�Ӧ���ʸ�����㣻����ͼ��������ʽ�����������Ӧ�Ƿ��ȷ�Ӧ����ѧƽ�����¶����ߣ�ƽ��������з�������ʵ����¶ȣ�
��� �⣺A��ʵ��1�ӿ�ʼ����Ӧ�ﵽ��ѧƽ��ʱ��
2SO2��g��+O2��g��?2SO3��g����
��ʼ����mol�� 4 2 0
�仯����mol�� 2.4 1.2 2.4
ƽ������mol�� x 0.8 2.4
x=4-2.4=1.6����A����
B�������������ݿ�֪��ʵ��1��ʵ��2��ʼ����ͬ��x=1.6��ʵ��2�ﵽƽ���������ı仯������ʵ��1������ʵ��2�൱��ʵ��1��Ӧ�����ƶ����÷�ӦΪ���ȷ�Ӧ�������ǽ����¶ȵĽ����ʵ��2�����ʵͣ�ʵ��2���¶ȵͣ���T2��T1����B��ȷ��
C���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ�������T2��T1������K2��K1����C����
D��ʵ��1��ǰ6 min�ķ�Ӧ����v��O2��=$\frac{2mol-0.8mol}{2L•6min}$=0.1 mol•L-1•min-1��v��SO2��=0.2 mol•L-1•min-1����D��ȷ��
��ѡBD��
���� ���⿼���˻�ѧƽ��Ӱ�����غ�ƽ�����ķ����жϣ�ע��֪ʶ��Ǩ�ƺ�Ӧ���ǽ���ؼ����ѶȲ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ���³�ѹ�£�11.2 LCO2������ԭ����Ϊ1.5NA | |
| B�� | ��״���£�22.4 L CCl4������������ΪNA | |
| C�� | ��״���£�18gˮ����ԭ����ΪNA | |
| D�� | ���³�ѹ�£�48 g O2��O3����ﺬ�е���ԭ����Ϊ3NA |
| A�� | ��Ԫ�ص��������ȼ�Ԫ�ص��������� | |
| B�� | �ס���Ԫ������������Ӧˮ���������ǿ��˳��Ϊ���ף��� | |
| C�� | ԭ�Ӱ뾶�ɴ�С��˳��Ϊ�������ף��� | |
| D�� | ����Ԫ�صĻ�������Ŀ�Ⱥ����Ԫ�صĻ�������Ŀ�� |
| A�� | Na��Mg��Al��ԭ�����μ��� | B�� | Cl2��Br2��I2������������ǿ | ||
| C�� | Be��Mg��Ca�����ᷴӦԽ��Խ���� | D�� | P��S��Cl��������������� |

| ���� | ��Է������� | �ܶȣ�g/mL�� | �е㣨�棩 | ˮ�� �ܽ��� |
| CHCl3 | 119.5 | 1.50 | 61.3 | ���� |
| CCl4 | 154 | 1.59 | 76.7 | ���� |
�ټ���װ�������ԣ��ڿ�ʼͨ��H2���۵�ȼB���ƾ��ƣ�
����A��ˮ���м�����ˮ����ͨC������װ�õ���ˮ����������ƿ�е���20mLCCl4����Ӧ������ֹͣ���ȣ���D����ƿ���ռ�����Һ��ֱ�������NaHCO3��Һ��ˮϴ�ӣ��ֳ��IJ������������ˮCaCl2���壬���ú���ˣ�
�߶���Һ�����������õ��ȷ�15g����ش�
��1��Aװ�õ�������Aװ�õ�������ʹ���������Ȼ�̼������ֻ�ϣ�
��2��������ںͲ���۵�˳��ߵ�����ʵ���в����IJ����������Ϊ_����ʱ����������������ը�������ɵ��ȷ±�������������
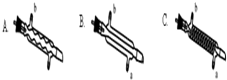
��3��B���з�����Ҫ��Ӧ�Ļ�ѧ����ʽΪCCl4+H2$��_{��}^{����}$CHCl3+HCl��
��4��C����Ӧѡ�õ�������ΪB����ѡ����ĸ������ˮӦ�Ӹ������ܵ�a���a����b�����ڽ��룮
��5��������У���ˮϴ�ӵ�Ŀ��Ϊϴ��NaHCO3��NaCl��
��6���ȷ��ڿ������ܱ�������������HCl������COCl2�����÷�Ӧ�Ļ�ѧ����ʽ2CHCl3+O2=2COCl2+2HCl��
��7����ʵ���У��ȷµIJ���Ϊ61%��
| �� ���� | IA | IIA | IIIA | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | �� | �� | ||||
| 3 | �� | �� | �� | �� | �� | �� | ⑪ | ⑫ |
��2��д���ࡢ������Ԫ�صķ��ţ�Si��P��
��3������ЩԪ���У�����õĽ��������ӽṹʾ��ͼ��
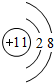 ������õķǽ���Ԫ����F ����Ԫ�ط��ţ���ͬ����Ar������õ�Ԫ�أ�
������õķǽ���Ԫ����F ����Ԫ�ط��ţ���ͬ����Ar������õ�Ԫ�أ���4����ЩԪ�ص�����������Ӧˮ�����У�HClO4���ѧʽ����ͬ��������ǿ��NaOH�ļ�����ǿ�����γ��������������Ԫ����Al����Ԫ�ط��ţ���
��5���ڢݵ�⑪��Ԫ���У�Cl����Ԫ�ط��ţ�ԭ�Ӱ뾶��С��
��6���ȽϢݺ͢Ļ�ѧ���ʣ�Na����Ԫ�ط��ţ������ã�����ʵ��֤��֮����������������ͽ��ۣ������������þ���ʷֱ�����ˮ��Ӧ����Ӧ���ҳ̶ȴ�����ƣ���֮��þ��
| A�� | ����ˮ�����ǻ�����Һ�к��е��������ࡢ��Ŀ��ͬ | |
| B�� | ����ˮ���д�����ͬ������ʵĵ��� | |
| C�� | ����ˮ�����д̼�����ζ������Ư���л�ɫ�� | |
| D�� | ����ˮ������ʱ��Ͼú�����Ϊ��ͬ��ԭ�������� |
| A�� | ���Ͼɵ����������Ͱ | B�� | ��ʵ���ҷ�Һ���н����������� | ||
| C�� | ����ֽ������ˮֱ���ŷ� | D�� | �ļ����յ��¶�������26������ |