题目内容
2.消除汽车尾气中的NO、CO,有利于减少PM2.5的排放.已知如下信息:N2(g)+O2(g)═2NO(g)△H1=+183kJ/mol
2CO(g)+O2(g)═2CO2(g)△H2=-565kJ/mol
在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-748kJ/mol.
分析 :①N2(g)+O2(g)═2NO(g)△H1=+183kJ/mol;
②2CO(g)+O2(g)═2CO2(g)△H2=-565kJ/mol
在催化剂作用下NO和CO转化为无毒气体,反应的热化学方程式依据盖斯定律计算②-①得.
解答 解:①N2(g)+O2(g)═2NO(g)△H1=+183kJ/mol;
②2CO(g)+O2(g)═2CO2(g)△H2=-565kJ/mol
在催化剂作用下NO和CO转化为无毒气体,反应的热化学方程式依据盖斯定律计算②-①得到:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-748 kJ/mol,
故答案为:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-748 kJ/mol.
点评 本题考查了热化学方程式书写方法,盖斯定律的应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
12.将一定量的SO2(g)和O2(g)分别通入体积为2 L的恒容密闭容器中,在不同温度下进行反应,得到如下表中的两组数据( )
| 实验 编号 | 温度 /℃ | 平衡常数 /mol-1•L | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| SO2 | O2 | SO2 | O2 | ||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
| A. | x=2.4 | |
| B. | T1、T2的关系:T1>T2 | |
| C. | K1、K2的关系:K2>K1 | |
| D. | 实验1在前6 min的反应速率v(SO2)=0.2 mol•L-1•min-1 |
13.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 气态氢化物的稳定性:W>Z | |
| D. | W的单质能与水反应,生成一种具有漂白性的物质 |
17.某温度下在容积不变的密闭容器中发生如下反应:2SO2+O2?2SO3(g),若开始时只充入2molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2mol SO2和1molO2的混合气体,达到平衡时SO2的转化率为( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
7.某同学利用如图1装置探究温度对化学平衡的影响,已知烧瓶中存在如下平衡:2NO2?N2O4△H<0.当进行图2实验后,以下结论正确的是( )
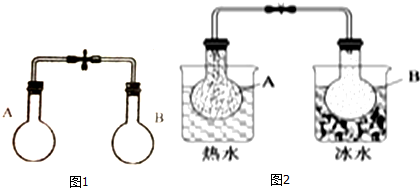

| A. | 图2中,B烧瓶颜色较深 | |
| B. | 图2中,B烧瓶与A烧瓶相比有较多的NO2 | |
| C. | 图2中B烧瓶的正反应速率比图1中B烧瓶的快 | |
| D. | 图2中A烧瓶的正反应速率比图1中A烧瓶的快 |
14.燃烧1g乙醇(液态)生成CO2气体和液态水放出热量为29.7KJ,则乙醇燃烧的热化学方程式正确的是( )
| A. | C2H 5OH+3O2═2CO2+3H 2O△H=-29.7 kJ/mol -1 | |
| B. | C2H 5OH(l)+3O2 (g)═2CO2 (g)+3H 2 O(l)△H=+1366.2kJ/mol -1 | |
| C. | C 2 H 5 OH(l)+3O2 (g)═2CO2 (g)+3H 2O(g)△H=+29.7 kJ/mol-1 | |
| D. | C2H 5OH(l)+3O2 (g)═2CO 2 (g)+3H 2 O(l)△H=-1366.2kJ/mol -1 |
12.W、X、Y、Z是中学化学常见的四种均含10个电子的微粒,它们之间的转化关系如下.下列叙述错误的是( )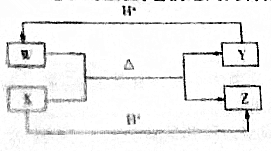

| A. | W的电子式为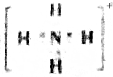 | |
| B. | Y与Z之间可形成氢键 | |
| C. | 硫酸与氢氧化钠溶液反应的离子方程式可表示为X+H+=Z | |
| D. | 微粒Y中各元素原子均达到8电子稳定结构 |
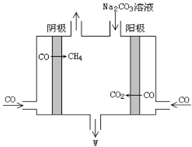 (1)利用CO2与H2反应可合成二甲醚(CH3OCH3).以KOH为电解质溶液,组成二甲醚--空气燃料电池,该电池工作时其负极反应式是CH3OCH3-12e-+16OH-=2CO32-+11H2O.
(1)利用CO2与H2反应可合成二甲醚(CH3OCH3).以KOH为电解质溶液,组成二甲醚--空气燃料电池,该电池工作时其负极反应式是CH3OCH3-12e-+16OH-=2CO32-+11H2O.