题目内容
把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是( )
| A、盐酸的浓度 |
| B、铝条的表面积 |
| C、溶液的温度 |
| D、加少量Na2SO4 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:过量稀盐酸,Al完全反应,不改变温度、接触面积、盐酸的浓度等,则不影响反应速率,以此来解答.
解答:
解:A.改变盐酸的浓度,反应速率变化,故A不选;
B.改变接触面积,反应速率变化,故B不选;
C.改变温度,反应速率变化,故C不选;
D.加少量Na2S04固体,对反应无影响,则Al与盐酸反应生成氢气的速率不变,故D选;
故选D.
B.改变接触面积,反应速率变化,故B不选;
C.改变温度,反应速率变化,故C不选;
D.加少量Na2S04固体,对反应无影响,则Al与盐酸反应生成氢气的速率不变,故D选;
故选D.
点评:本题考查影响反应速率的因素,明确温度、浓度、接触面积对反应速率的影响即可解答,注意反应的实质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
钢铁腐蚀发生得最普遍的是( )
| A、化学腐蚀 | B、析氢腐蚀 |
| C、吸氧腐蚀 | D、摩擦 |
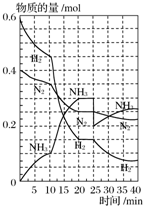 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图所示,下列说法中正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图所示,下列说法中正确的是( )| A、从反应开始到第一次平衡时,N2的平均反应速率为0.005 mol?L-1?min-1 |
| B、平衡在10 min至20 min的变化,可能是因为增大了容器体积 |
| C、25 min时,分离出了0.1 mol NH3 |
| D、在25 min后平衡向正反应方向移动,新平衡中NH3的体积分数比原平衡的小 |
有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
| A、若有l mol NO3-参加还原反应,则转移8mol e- |
| B、还原产物为NH4+ |
| C、氧化剂与还原剂的物质的量之比为8:l |
| D、若把该反应设计为原电池,则负极反应为Fe 2+-e-=Fe 3+ |
下列溶液中,Na+数目最多的是( )
| A、1 mol?L-1 Na2SO4溶液100mL |
| B、0.9 mol?L-1Na3PO4溶液100mL |
| C、2.5 mol?L-1NaOH 溶液100mL |
| D、1 mol?L-1 NaHCO3溶液100mL |
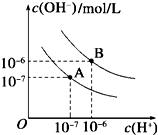 水的电离平衡线如图所示.
水的电离平衡线如图所示.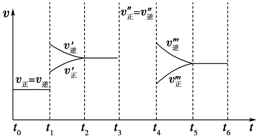 密闭容器中发生如下反应:A(g)+3B(g)?2C(g)△H<0,根据下列速率-时间图象,回答下列问题.
密闭容器中发生如下反应:A(g)+3B(g)?2C(g)△H<0,根据下列速率-时间图象,回答下列问题. 某校研究性学习小组就氮及其化合物展开研究.
某校研究性学习小组就氮及其化合物展开研究.