题目内容
20.室温时,将浓度和体积分别为c1,V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是( )| A. | 当pH=7时,若V1=V2,则一定是c2>c1 | |
| B. | 在任何情况下都满足c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 若pH>7,则一定是c1V1>c2V2 | |
| D. | 若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
分析 A.醋酸钠溶液呈碱性,pH=7时溶液呈中性,醋酸物质的量应该稍微大些;
B.任何电解质溶液中都存在电荷守恒,结合溶液中含有离子判断;
C.醋酸钠是强碱弱酸盐,其溶液呈碱性,如果混合溶液pH>7,溶液中溶质可能为醋酸钠,也可能为醋酸钠和少量醋酸,或者醋酸钠和氢氧化钠;
D.根据物料守恒判断.
解答 解:A.醋酸钠是强碱弱酸盐,其溶液呈碱性,如果混合溶液pH=7,溶液呈中性,醋酸物质的量应该稍微大些,即c1V1<c2V2,若V1=V2,则一定是c2>c1,故A正确;
B.电解质溶液呈电中性,根据电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故B正确;
C.醋酸钠是强碱弱酸盐,其溶液呈碱性,如果混合溶液pH>7,溶液中溶质可能为醋酸钠,也可能为醋酸钠和少量醋酸,或者醋酸钠和氢氧化钠,当pH>7时,可能c1V1=c2V2,也可能是c1V1<c2V2,或者c1V1>c2V2,故D错误;
D.若V1=V2,c1=c2,两溶液中溶质NaOH与醋酸的物质的量相等,根据物料守恒得c(CH3COO-)+c(CH3COOH)=c(Na+),故D正确;
故选C.
点评 本题考查酸碱混合溶液定性判断及离子浓度大小比较,注意任何电解质溶液中都存在电荷守恒和物料守恒,注意溶质组成与溶液酸碱性关系的判断.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
10.如图是有关电化学的图示,完全正确的是( )
| A. | 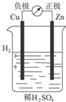 Cu-Zn原电池 | B. | 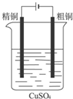 粗铜的精炼 | C. | 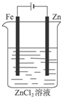 铁片镀锌 | D. | 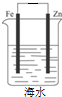 减缓铁腐蚀 |
8.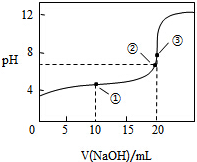 常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图,下列说法不正确的是( )
常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图,下列说法不正确的是( )
 常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图,下列说法不正确的是( )
常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图,下列说法不正确的是( )| A. | 点③溶液显碱性的原因是 CH3COO-+H2O═CH3COOH+OH- | |
| B. | 点②时溶液中c(Na+)大于c(CH3COO-) | |
| C. | 点①溶液中 c(CH3COOH)+c(H+)>c(CH3COO-)+c(OH-) | |
| D. | 在逐滴加入NaOH溶液至40mL的过程中,水的电离程度先增大后减小 |
15.25℃时下列叙述不正确的是( )
| A. | pH=3的二元弱酸H2R溶液与p=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液中:2c(R2-)+c(HR-)=(Na+) | |
| B. | 若0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合后,溶液的pH=9,则:c(OH-)-c(HY)=(H+)=1×10-9mol•L-1 | |
| C. | 0.2mol•L-1HCl溶液与等体积0.05mol•L-1Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | 0.1mol•L-1Na2S与0.1mol•L-1NaHS等体积混合:3c(Na+)-2c(HS-)=2c(S2-)+2c(H2S) |
5.常温下,醋酸和氨水的电离平衡常数均为1.8×10-5.向10mL浓度为0.1mol•L-1的NH3•H2O溶液中滴加相同浓度的CH3COOH(温度变化忽略不计),在滴加过程中( )
| A. | $\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$先增大再减小 | |
| B. | c(NH4+)与c(NH3•H2O)之和始终保持不变 | |
| C. | 水的电离程度始终增大 | |
| D. | 当加入CH3COOH的体积为10mL时,c(NH4+)=c(CH3COO-) |
9.常温下pH为2的盐酸,下列叙述正确的是( )
| A. | 将10 mL该溶液稀释至100 mL后,pH=4 | |
| B. | 向该溶液中加入等体积pH为12的氨水恰好完全中和 | |
| C. | 该溶液中盐酸电离出的c(H+)与水电离出的c(H+)之比为1010:1 | |
| D. | 该溶液中由水电离出的c(H+)水×c(OH-)水=1×10-14 |
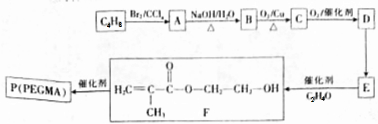
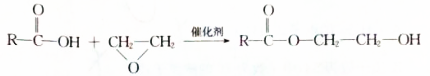
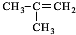 .
.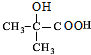 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$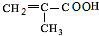 +H2O,该反应的反应类型是消去反应.
+H2O,该反应的反应类型是消去反应.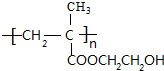 .
.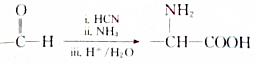 .设计由B合成
.设计由B合成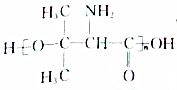 的路线.合成路线流程图请参考如下形式.
的路线.合成路线流程图请参考如下形式.
 .
.
