题目内容
已知:
(1)
(2)
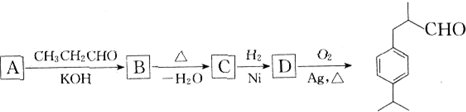
甲苯及其卤代物是有机化工的基本原料,由它出发可制造某些香料、药物及广泛应用于印刷、电子工业中的感光树脂的重要中间体,它们之间的关系如下图所示:

图中 B、D、E 都能使溴水褪色,E 在光等辐射能作用下可以发生二聚加成反应,
生成互为同分异构体的环状化合物 F 和 G; E 还可以在一定条件下形成一种优质高分子感光树脂的单体H.试回答:
(1)写出有机物的结构简式:A 、C 、D .
(2)反应(Ⅰ)的类型是 ,反应(Ⅱ)的类型是 .
(3)完成化学方程式:A→B: .
(4)同种类、互为同分异构体的 F 和 G 的结构简式为:F 、G .
(5)已知: ,如果E→H的反应在一定条件下也能实现的话,请你预测所得高分子感光树脂单体H 的最简单的结构简式为 .
,如果E→H的反应在一定条件下也能实现的话,请你预测所得高分子感光树脂单体H 的最简单的结构简式为 .
(1)

(2)

甲苯及其卤代物是有机化工的基本原料,由它出发可制造某些香料、药物及广泛应用于印刷、电子工业中的感光树脂的重要中间体,它们之间的关系如下图所示:

图中 B、D、E 都能使溴水褪色,E 在光等辐射能作用下可以发生二聚加成反应,
生成互为同分异构体的环状化合物 F 和 G; E 还可以在一定条件下形成一种优质高分子感光树脂的单体H.试回答:
(1)写出有机物的结构简式:A
(2)反应(Ⅰ)的类型是
(3)完成化学方程式:A→B:
(4)同种类、互为同分异构体的 F 和 G 的结构简式为:F
(5)已知:
 ,如果E→H的反应在一定条件下也能实现的话,请你预测所得高分子感光树脂单体H 的最简单的结构简式为
,如果E→H的反应在一定条件下也能实现的话,请你预测所得高分子感光树脂单体H 的最简单的结构简式为考点:有机物的推断
专题:有机物的化学性质及推断
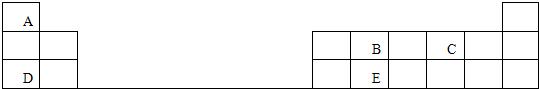
分析: 和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是
和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是 ,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为:
,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为: ,B与银氨溶液反应,然后酸化生成E,则E的结构简式为:
,B与银氨溶液反应,然后酸化生成E,则E的结构简式为: ,E和甲醇发生酯化反应生成J,J的结构简式为:
,E和甲醇发生酯化反应生成J,J的结构简式为: ,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为
,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为 、
、 中的一种;1molB与2mol氢气发生加成反应生成C,则C为
中的一种;1molB与2mol氢气发生加成反应生成C,则C为 ,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为
,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为 ,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为:
,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为: .
.
 和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是
和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是 ,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为:
,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为: ,B与银氨溶液反应,然后酸化生成E,则E的结构简式为:
,B与银氨溶液反应,然后酸化生成E,则E的结构简式为: ,E和甲醇发生酯化反应生成J,J的结构简式为:
,E和甲醇发生酯化反应生成J,J的结构简式为: ,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为
,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为 、
、 中的一种;1molB与2mol氢气发生加成反应生成C,则C为
中的一种;1molB与2mol氢气发生加成反应生成C,则C为 ,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为
,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为 ,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为:
,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为: .
.解答:
解: 和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是
和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是 ,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为:
,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为: ,B与银氨溶液反应,然后酸化生成E,则E的结构简式为:
,B与银氨溶液反应,然后酸化生成E,则E的结构简式为: ,E和甲醇发生酯化反应生成J,J的结构简式为:
,E和甲醇发生酯化反应生成J,J的结构简式为: ,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为
,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为 、
、 中的一种;1molB与2mol氢气发生加成反应生成C,则C为
中的一种;1molB与2mol氢气发生加成反应生成C,则C为 ,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为
,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为 ,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为:
,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为: ,
,
(1)通过以上分析知,A为 、C为
、C为 ,D为
,D为 ,
,
故答案为: ;
; ;
; ;
;
(2)反应(Ⅰ)是甲苯氧化生成苯甲醛,反应(Ⅱ)是E( )和甲醇发生酯化反应生成
)和甲醇发生酯化反应生成 ,
,
故答案为:氧化反应;酯化反应;
(3)A→B的反应方程式为: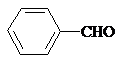 +CH3CHO
+CH3CHO
 +H2O,
+H2O,
故答案为: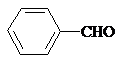 +CH3CHO
+CH3CHO
 +H2O;
+H2O;
(4)E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为 、
、 中的一种,
中的一种,
故答案为: ;
; ;
;
(5)中E和乙炔反应生成H,由信息可知,H的结构简式为: ,
,
故答案为: .
.
 和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是
和氢氧化钠的水溶液发生水解反应生成A,A能发生银镜反应,则A中含有醛基,根据题给信息知,A是 ,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为:
,苯甲醛和乙醛反应生成B,根据题给信息知,B的结构简式为: ,B与银氨溶液反应,然后酸化生成E,则E的结构简式为:
,B与银氨溶液反应,然后酸化生成E,则E的结构简式为: ,E和甲醇发生酯化反应生成J,J的结构简式为:
,E和甲醇发生酯化反应生成J,J的结构简式为: ,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为
,E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为 、
、 中的一种;1molB与2mol氢气发生加成反应生成C,则C为
中的一种;1molB与2mol氢气发生加成反应生成C,则C为 ,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为
,B发生还原反应生成D,D能使溴水褪色、不能发生银镜反应,可推知B中醛基发生还原反应,故D为 ,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为:
,(5)中E和乙炔反应生成H,由信息可知,H的结构简式为: ,
,(1)通过以上分析知,A为
 、C为
、C为 ,D为
,D为 ,
,故答案为:
 ;
; ;
; ;
;(2)反应(Ⅰ)是甲苯氧化生成苯甲醛,反应(Ⅱ)是E(
 )和甲醇发生酯化反应生成
)和甲醇发生酯化反应生成 ,
,故答案为:氧化反应;酯化反应;
(3)A→B的反应方程式为:
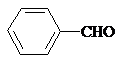 +CH3CHO
+CH3CHO| 稀OH- |
 +H2O,
+H2O,故答案为:
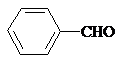 +CH3CHO
+CH3CHO| 稀OH- |
 +H2O;
+H2O;(4)E 在光等辐射能作用下可以发生二聚加成反应,得到F与G,它们的结构分别为
 、
、 中的一种,
中的一种,故答案为:
 ;
; ;
;(5)中E和乙炔反应生成H,由信息可知,H的结构简式为:
 ,
,故答案为:
 .
.
点评:本题考查了有机物的推断,需要对给予的信息进行利用,能较好的考查学生的自学能力、阅读能力、逻辑推理能力等,正确理解题给信息是解本题关键,采用正推的方法进行分析解答,注意醛基发生加成反应时其断键方式,为易错点,难度中等.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
在水溶液中能大量共存的一组是( )
| A、Ba2+、Na+、SO32-、Cl- |
| B、MnO4-、SO42-、K+、H+ |
| C、Al3+、Mg2+、NO3-、HCO3- |
| D、Fe3+、Na+、SCN-、Cl- |
放射性同位素12553I可用于治疗肿瘤.12553I的原子核内的中子数为( )
| A、125 | B、72 | C、53 | D、19 |
 [化学--选修物质结构与性质]
[化学--选修物质结构与性质] ,由短周期元素构成的与SO
,由短周期元素构成的与SO
 )在食品、化妆品等工业中用作香料添加剂.其合成流程为(部分产物及反应条件已略去,键线式参见本试卷第12题):
)在食品、化妆品等工业中用作香料添加剂.其合成流程为(部分产物及反应条件已略去,键线式参见本试卷第12题):