题目内容
6.与30mL 1mol/LAlCl3溶液中c(Cl-)相等的是( )| A. | 50mL 3mol/L的KCl溶液 | B. | 30mL 1mol/L的NaCl溶液 | ||
| C. | 30mL 3mol/L的FeCl3溶液 | D. | 10mL3mol/L的AlCl3溶液 |
分析 离子的物质的量浓度=溶质的物质的量浓度×每个化学式中含有的离子个数,与溶液的体积无关.
解答 解:30mL 1mol/LAlCl3溶液中c(Cl-)=1mol/L×3=3mol/L;
A.3mol/LKCl溶液中c(Cl-)=3mol/L×1=3mol/L,故A正确;
B.2mol/LNH4Cl溶液溶液中c(Cl-)=2mol/L×1=2mol/L,故B错误;
C.1.5mol/LFeCl3溶液中所含c(Cl-)=3mol/L×3=9mol/L,故C错误;
D.10mL3mol/L的AlCl3溶液中c(Cl-)=3mol/L×3=9mol/L,故D错误;
故选A.
点评 本题考查物质的量浓度的计算,明确浓度与物质的构成的关系是解答本题的关键,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.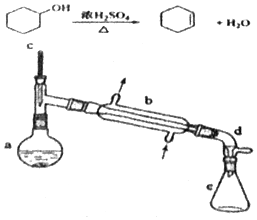 分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:
分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:
可能用到的有关数据如下:
Ⅰ.合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1ml浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是冷凝管.
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)分离提纯过程中加入无水氯化钙的目的是干燥.
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有C(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶.
 分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:
分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:可能用到的有关数据如下:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1ml浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是冷凝管.
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)分离提纯过程中加入无水氯化钙的目的是干燥.
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有C(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶.
14.可以用于鉴别淀粉溶液和蛋白质溶液的方法是( )
| A. | 分别加入碘化钾溶液,观察颜色变化 | |
| B. | 分别加热,观察是否生成沉淀 | |
| C. | 分别滴加浓硝酸 | |
| D. | 分别灼烧,闻味道 |
1.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g)△H1=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
| A. | 碳的燃烧热为221KJ/mol | |
| B. | 稀盐酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热值为57.3KJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ |
11.摩尔是( )
| A. | 国际单位制的一个基本物理量 | B. | 表示物质质量的单位 | ||
| C. | 物质的量的单位 | D. | 表示物质数量的单位 |
18.下列不属于自发进行的变化是( )
| A. | 红墨水加到清水使整杯水变红 | B. | 冰在室温下融化成水 | ||
| C. | 水电解生成氢气和氧气 | D. | 铁器在潮湿的空气中生锈 |
7. 实验室制取乙酸乙酯的主要步骤如下
实验室制取乙酸乙酯的主要步骤如下
①在25mL的大试管A中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合溶液.
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min.
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置分层.
④分离出乙酸乙酯层、洗涤、干燥.
以下数据可供参考:
按要求回答下列问题,
(1)配制该混合液试剂的添加顺序为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加冰醋酸.
(2)写出该反应的化学方程式:CH3COOH+CH3CH2OH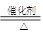 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.
(3)该反应中哪些措施可以提高乙酸的转化率CD.
A.使用碎瓷片 B.酒精灯加热C.浓硫酸作吸水剂 D.将生成的乙酸乙酯蒸出
(4)上述实验中饱和碳酸钠溶液的主要是BCD(填字母)
A.加速酯的生成,提高其产率
B.降低乙酸乙酯的溶解度,便于液体分层
C.中和蒸出来的乙酸
D.吸收蒸出来的乙醇
(5)步骤②中需要小火均匀加热操作,其主要理由是:①温度过高可能发生其他副反应②减少乙酸乙醇的挥发.
(6)分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤,通过洗涤出去碳酸钠、乙醇;为了干燥乙酸乙酯可选用的干燥剂为B(填字母).
A.浓硫酸 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
 实验室制取乙酸乙酯的主要步骤如下
实验室制取乙酸乙酯的主要步骤如下①在25mL的大试管A中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合溶液.
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min.
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置分层.
④分离出乙酸乙酯层、洗涤、干燥.
以下数据可供参考:
| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 | 浓硫酸 |
| 熔(℃) | -117.0 | 16.6 | -83.6 | ------ |
| 沸(℃) | 78.0 | 117.9 | 77.5 | 338.0 |
(1)配制该混合液试剂的添加顺序为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加冰醋酸.
(2)写出该反应的化学方程式:CH3COOH+CH3CH2OH
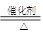 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.(3)该反应中哪些措施可以提高乙酸的转化率CD.
A.使用碎瓷片 B.酒精灯加热C.浓硫酸作吸水剂 D.将生成的乙酸乙酯蒸出
(4)上述实验中饱和碳酸钠溶液的主要是BCD(填字母)
A.加速酯的生成,提高其产率
B.降低乙酸乙酯的溶解度,便于液体分层
C.中和蒸出来的乙酸
D.吸收蒸出来的乙醇
(5)步骤②中需要小火均匀加热操作,其主要理由是:①温度过高可能发生其他副反应②减少乙酸乙醇的挥发.
(6)分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤,通过洗涤出去碳酸钠、乙醇;为了干燥乙酸乙酯可选用的干燥剂为B(填字母).
A.浓硫酸 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
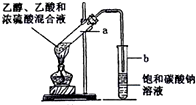 如图为实验室制取乙酸乙酯的装置.
如图为实验室制取乙酸乙酯的装置. CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O