题目内容
1.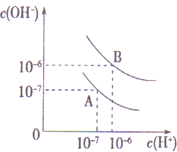 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:(1)则25℃时水的电离平衡曲线应为A(填“A”或“B”)
(2)95℃时,若100体钗pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸pH1的与强碱的pH2之间应满足的关系是pH1+pH2=14(或a+b=14).
分析 (1)横轴是氢离子浓度,纵轴是氢氧根离子浓度,水的离子积常数Kw=c(H+)×c(OH-)计算出A曲线的Kw,然后结合水的电离过程吸热判断25℃时水的电离平衡曲线;
(2)酸、碱都是强电解质,溶液呈中性说明氢离子和氢氧根离子的物质的量相等,结合水的离子积常数确定强酸的pH1与强碱的pH2之间应满足的关系.
解答 解:(1)曲线A条件下Kw=c(H+)×c(OH-)=10-7×10-7=10-14,曲线B条件下c(H+)=c(OH-)=10-6 mol/L,Kw=c(H+)•c(OH-)=10-12,水的电离时吸热过程,加热促进电离,所以A曲线代表25℃时水的电离平衡曲线,
故答案为:A;
(2)要注意的是95°C时,水的离子积为10-12,即酸、碱浓度相等时pH(酸)+pH(碱)=12,现强碱的OH-浓度是强酸H+浓度的100倍,所以pH(酸)+pH(碱)=14,即pH1+pH2=14,或a+b=14,
故答案为:pH1+pH2=14(或a+b=14).
点评 本题考查了溶液酸碱性与溶液pH的计算,题目难度中等,明确弱电解质的电离及其影响为解答关键,注意掌握溶液酸碱性与溶液pH的关系及计算方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
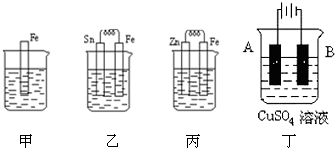
12.下列对碱性锌锰电池的叙述不 正确的是( )
| A. | 锌是正极,MnO2是负极 | |
| B. | 电解质是KOH溶液 | |
| C. | 锌发生氧化反应,MnO2发生还原反应 | |
| D. | 它的能量和储存时间比普通锌锰电池高 |
16.如图所示,甲池的总反应式为 2CH3OH+3O2+4KOH═2K2CO3+6H2O.下列说法正确的 是( )
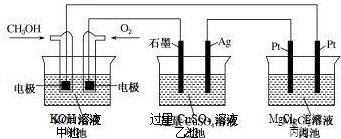

| A. | 若将乙池电解液换成 AgNO3 溶液,则可以实现在石墨棒上镀银 | |
| B. | 甲池通入 CH3OH 的电极反应式为 CH3OH+6e-+2H2O═CO32-+8H+ | |
| C. | 反应一段时间后,向乙池中加入一定量 Cu(OH)2 固体,能使 CuSO4溶液恢复到 原浓度 | |
| D. | 甲池中消耗 224mL(标准状况下)O2,此时丙池中理论上产生 1.16g 固体 |
6.下列溶液或浊液中,关于离子浓度的说法正确的是( )
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值增大 | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3、NaHCO3混合溶液中:c(CO32-)>c(HCO3-),且2c(Na+)=3c(H2CO3)+3c(HCO3-)+3c(CO32-) | |
| C. | 常温下0.4 mol•L-1 HB溶液和0.2 mol•L-1 NaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系:c(Na+)>c(B-)>c(HB)>c(H+)>c(OH-) | |
| D. | 假设HClO的电离平衡常数为Ka,碳酸的电离常数分别记为:Ka1和Ka2,已知:Ka1>Ka>Ka2,则发生反应:2NaClO+CO2(少量)+H2O═Na2CO3+2HClO |
10.实验是研究化学的基础,下列有关实验的方法、装置或操作都正确的是( )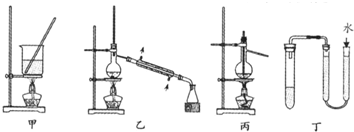

| A. | 用甲装置将海带灼烧成灰 | |
| B. | 分离Na2CO3溶液和CH3COOC2H5,可使用如图乙所示实验装置 | |
| C. | 利用丙装置进行石油分馏 | |
| D. | 利用丁装置检验装置的气密性 |
11.下列过程不需要通电就能进行的是①电离②电解③电镀④电化学腐蚀( )
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |