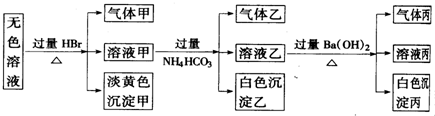
题目内容
现有铜质印刷线路板浸入200 mL氯化铁溶液中,有6.4g铜被腐蚀掉.取出印刷线路板,向溶液中加入5.6 g铁粉,经充分反应后,溶液中还存在3.2g不溶物.下列说法正确的是( )
| A、3.2 g不溶物为铁、铜混合物 |
| B、加铁粉之前,溶液中存在的金属阳离子有Cu2+、Fe3+ |
| C、加铁粉之前,溶液中的c(Cu2+):c(Fe2+)=1:1 |
| D、反应结束后溶液中的c(Fe2+)=2 mol?L-1 |
考点:有关混合物反应的计算
专题:
分析:A.依据反应:Cu+2FeCl3═CuCl2+2FeCl2、Fe+CuCl2=FeCl2+Cu判断溶液中剩余的金属离子、固体物质的成分;
B.根据A的分析判断加铁粉之前,溶液中存在的金属阳离子;
C.根据铜的物质的量计算出铜离子的物质的量,加入铁粉后置换出部分铜,说明加入铁粉前铁离子有剩余,则铜完全与铁离子反应,据此可知铜离子与亚铁离子浓度之比;
D.根据铁元素守恒计算出反应结束后溶液中铁离子的浓度.
B.根据A的分析判断加铁粉之前,溶液中存在的金属阳离子;
C.根据铜的物质的量计算出铜离子的物质的量,加入铁粉后置换出部分铜,说明加入铁粉前铁离子有剩余,则铜完全与铁离子反应,据此可知铜离子与亚铁离子浓度之比;
D.根据铁元素守恒计算出反应结束后溶液中铁离子的浓度.
解答:
解:A.加入Fe粉前,溶液中有Cu2+,Fe2+,Cl-,可能还有Fe3+,5.6gFe为0.1mol,6.4gCu为0.1mol,若无Fe3+,那么Fe恰好把5.6gCu全部置换出来,现在只有3.2g不容物,所以固体不可能为Fe,只能是Cu,故A错误;
B.根据A可知,加入铁粉前原溶液中含有Cu2+、Fe2+、Fe3+,故B错误;
C.加入铁粉前溶液中铜离子的物质的量为0.1mol,加入铁粉的物质的量为0.1mol,置换出的铜的物质的量为0.05mol,则与剩余铁离子反应的铁的物质的量为0.05mol,所以加入铁粉之前溶液中亚铁离子的物质的量为:0.1mol×2-0.2mol,则加入铁粉前c(Cu2+):c(Fe2+)=0.1mol:0.2mol=1:2,故C错误;
D.加入0.1mol铁粉后置换出0.05mol铜,说明原溶液中铁离子置换出亚铁离子总共消耗了0.1mol铁、0.05mol铜,所以原溶液中铁离子的物质的量为:0.1mol×2+0.05mol×2=0.3mol,根据铁元素守恒可知,反应后亚铁离子的物质的量为:0.3mol+0.1mol=0.4mol,反应结束后溶液中亚铁离子浓度为:
=2mol/L,故D正确;
故选D.
B.根据A可知,加入铁粉前原溶液中含有Cu2+、Fe2+、Fe3+,故B错误;
C.加入铁粉前溶液中铜离子的物质的量为0.1mol,加入铁粉的物质的量为0.1mol,置换出的铜的物质的量为0.05mol,则与剩余铁离子反应的铁的物质的量为0.05mol,所以加入铁粉之前溶液中亚铁离子的物质的量为:0.1mol×2-0.2mol,则加入铁粉前c(Cu2+):c(Fe2+)=0.1mol:0.2mol=1:2,故C错误;
D.加入0.1mol铁粉后置换出0.05mol铜,说明原溶液中铁离子置换出亚铁离子总共消耗了0.1mol铁、0.05mol铜,所以原溶液中铁离子的物质的量为:0.1mol×2+0.05mol×2=0.3mol,根据铁元素守恒可知,反应后亚铁离子的物质的量为:0.3mol+0.1mol=0.4mol,反应结束后溶液中亚铁离子浓度为:
| 0.4mol |
| 0.2L |
故选D.
点评:本题考查了有关混合物反应的计算,题目难度中等,根据题中数据正确判断加入铁粉前溶液中含有的金属阳离子组成为解答关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
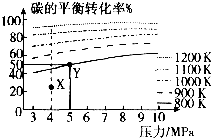 已知给煤炭加氢可发生反应:C(s)+2H2(g)?CH4(g).在VL的容器中投入amol碳(足量),同时通入2amolH2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示.下列说法正确的是( )
已知给煤炭加氢可发生反应:C(s)+2H2(g)?CH4(g).在VL的容器中投入amol碳(足量),同时通入2amolH2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示.下列说法正确的是( )| A、上述正反应为放热反应 | ||
| B、在4MPa、1200K时,图中X点v(H2)正>v(H2)逆 | ||
C、在5MPa、800K时,该反应的平衡常数为
| ||
| D、工业上维持6MPa1000K而不采用10MPa1000K,主要是因为前者碳的转化率高 |
下列对非金属元素(除稀有气体元素外)的相关判断正确的是( )
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价.
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价.
| A、②⑤ | B、①③⑤ |
| C、②③④ | D、①⑤ |
以下说法正确的是( )
| A、少量的金属钠长期暴露在空气中,它的最终产物是NaHCO3 |
| B、向紫色石蕊溶液中加入过量Na2O2粉末,振荡,产生气泡,溶液仍为紫色 |
| C、CO与H2混合气体3 g和足量的氧气燃烧后,在150℃时将混合气体通过足量的Na2O2后,Na2O2增重的质量为3g |
| D、将1g Na2CO3和NaHCO3分别溶于10mL水中,滴入酚酞试液后溶液所显红色深浅相同 |
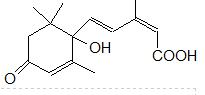 S-诱抗素的分子结构如图,下列关于该分子含有的官能团说法正确的是( )
S-诱抗素的分子结构如图,下列关于该分子含有的官能团说法正确的是( )| A、含有碳碳双键、羟基、羧基 |
| B、含有苯环、羟基、碳碳双键、羧基 |
| C、该物质能与烧碱溶液反应,但不能与纯碱溶液反应 |
| D、该物质为两性物质 |