题目内容
8.下列说法中,正确的是( )| A. | 44 g CO2的体积是22.4 L | |
| B. | NH3的摩尔质量是17g/mol | |
| C. | 100 mL 1 mol/L NaCl溶液中含有1 mol Cl- | |
| D. | 标准状况下,11.2 L H2O中含有3.01×1023个水分子 |
分析 A、状况不知,无法求体积;
B、氨气的相对分子质量是17;
C、根据n=cV进行计算求解;
D、水是液体.
解答 解:A、状况不知,无法求体积,故A错误;
B、氨气的相对分子质量是17,所以NH3的摩尔质量是17g/mol,故B正确;
C、n=cV=0.1L×1 mol/L=0.1mol,所以含有0.1 mol Cl-,故C错误;
D、水是液体,无法由体积求物质的量,故D错误;
故选B.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用,注意对化学式意义的理解.

练习册系列答案
相关题目
19.下列图示与对应的叙述相符的是( )
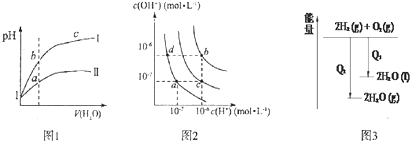

| A. | 图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 | |
| B. | 图2中纯水仅升高温度,就可以从a点变到c点 | |
| C. | 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 | |
| D. | 图3表示氢气与氧气反应中的能量变化 |
16.电解质是一类在水溶液里或熔融状态下能够导电的化合物.下列物质属于电解质的是( )
| A. | Fe | B. | NaCl | C. | SiO2 | D. | KNO3溶液 |
3.下列反应属于取代反应的是( )
| A. | 甲烷与氯气反应生成一氯甲烷 | B. | 苯与氢气反应生成环己烷 | ||
| C. | 乙烯与溴反应生成1,2-二溴乙烷 | D. | 乙醇与氧气反应生成乙醛 |
20.含汞废水主要来源于氯碱工业和塑料工业,未经处理不得排放.某含汞酸性废水(主要含Hg2+、H+、Na+、Cl-等)的处理工艺流程如图所示.
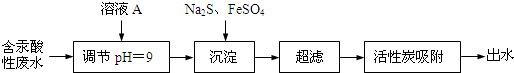
请回答:
(1)含汞废水未经处理直接排放的危害是(填字母)ab.
a.造成水体污染 b.引起人体中毒
(2)调节废水pH时加入的溶液A可能是(填字母)b.a.盐酸b.NaOH溶液
(3)Na2S与Hg2+发生反应的离子方程式是S2-+Hg2+=HgS↓.
(4)该废水经处理后,测得有关数据如下(其他离子忽略不计):
则c(Fe2+)=2.0×10-4mol/L.

请回答:
(1)含汞废水未经处理直接排放的危害是(填字母)ab.
a.造成水体污染 b.引起人体中毒
(2)调节废水pH时加入的溶液A可能是(填字母)b.a.盐酸b.NaOH溶液
(3)Na2S与Hg2+发生反应的离子方程式是S2-+Hg2+=HgS↓.
(4)该废水经处理后,测得有关数据如下(其他离子忽略不计):
| 离子 | Na+ | Fe2+ | Cl- | SO42- |
| 浓度(mol/L) | 3.0×10-4 | 2.0×10-4 | 2.5×10-4 |
17. 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )| A. | 溶液中的阳离子只有H+、NH4+、Mg2+、Al3+ | |
| B. | 溶液中n(NH4+)=0.2mol | |
| C. | 溶液中一定不含CO32-,可能含有SO42-和NO3- | |
| D. | n(H+):n(Al3+):n(Mg2+)=1:1:1 |
18.下列关于饱和食盐水的用途及装置设计正确的是( )
| A. | 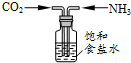 a-模拟工业制纯碱 | B. | 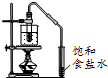 b-制乙酸乙酯实验中接受产物 | ||
| C. | 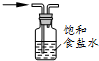 c-除去氯气中的氯化氢 | D. | 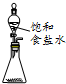 d-实验室制乙炔 |