题目内容
10.如图是氢氧燃料电池结构示意图,下列关于该电池的说法中,正确的是( )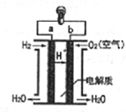
| A. | b极是负极 | B. | 正极发生氧化反应 | ||
| C. | a极的电极反应是H2-2e-=2H+ | D. | 该电池工作时,有淡蓝色火焰产生 |
分析 A.燃料电池中,通入燃料的电极为负极;
B.氢氧燃料原电池的正极上是氧气得电子的还原反应;
C.燃料电池中,通入燃料的电极为负极,发生失电子的氧化反应;
D.该电池工作时,氢氧燃料电池反应式与氢气燃烧方程式相同,但是现象不同.
解答 解:A.燃料电池中,通入燃料的电极为负极,所以a是负极,故A错误;
B.氢氧燃料原电池的正极上是氧气得电子的还原反应,故B错误;
C.燃料电池中,通入燃料的电极为负极,所以a是负极,电极反应是H2-2e-=2H+,故C正确;
D.该电池工作时,氢氧燃料电池反应式与氢气燃烧方程式相同,则电池反应式为2H2+O2═2H2O,但是不会出现燃烧现象,没有淡蓝色火焰产生,故D错误;
故选C.
点评 本题考查了原电池原理,根据原电池概念、燃料电池中得失电子、电极反应等知识点来分析解答即可,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
20.在已经处于化学平衡状态的体系中,如果下列量发生变化,化学平衡一定会移动的是( )
| A. | 反应物和生成物的浓度改变 | B. | 反应体系的压强改变 | ||
| C. | 正、逆反应的速率改变 | D. | 反应物的转化率改变 |
18.我国科学家发现了一种新核素${\;}_{80}^{208}$Hg,它的中子数为( )
| A. | 288 | B. | 208 | C. | 80 | D. | 128 |
5.下列粒子中,与H2O具有相同电子数的是( )
| A. | N2 | B. | S2- | C. | NH4+ | D. | HCl |
15.下列有关说法中,正确的是( )
| A. | 第1A族均为碱金属元素 | |
| B. | 最外层有两个电子的原子一定在第ⅡA族 | |
| C. | 元素的最高化合价等于其原子的最外层电子数 | |
| D. | 第ⅦA族元素的阴离子还原性越强,其气态氢化物的稳定性越弱 |
2.常温下,某酸HA的电离常数Ka=1×10-5,下列说法正确的是( )
| A. | 向HA溶液中逐滴加入少量NH3•H2O,$\frac{c({H}^{+})}{c({A}^{-})}$逐渐增大 | |
| B. | 常温下,0.1mol•L-1 HA溶液中水电离的c(H+)为10-13mol•L-1 | |
| C. | NaA溶液中加入HCl溶液至恰好完全反应,存在关系:2c(Na+)=c(A-)+c(Cl-) | |
| D. | 常温下,0.1mol•L-1 NaA溶液水解常数为10-9 |
19.短期元素X、Y、Z在周期表中的位置如图所示,则下列说法正确的是( )


| A. | X、Y、Z中Z的单质最稳定 | B. | Y的氢化物为H2Y | ||
| C. | H2Z能发生反应:Cl2+H2Z=Z+2HCl | D. | Y有含氧酸为HYO |
20.钯(Pd)元素的原子序数为46,下列叙述错误的是( )
| A. | ${\;}_{46}^{102}$Pd和${\;}_{46}^{103}$Pd互为同位素 | |
| B. | 钯是第五周期元素 | |
| C. | Pd2+核外有48个电子 | |
| D. | ${\;}_{62}^{108}$Pd的原子核内有62个中子 |
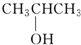 ⑨${\;}_{6}^{13}$C (填序号)
⑨${\;}_{6}^{13}$C (填序号)