题目内容
15.下列有关说法中,正确的是( )| A. | 第1A族均为碱金属元素 | |
| B. | 最外层有两个电子的原子一定在第ⅡA族 | |
| C. | 元素的最高化合价等于其原子的最外层电子数 | |
| D. | 第ⅦA族元素的阴离子还原性越强,其气态氢化物的稳定性越弱 |
分析 A、第ⅠA族元素除碱金属外还包括氢元素;
B、氦最外层2个电子;
C、O、F无正价;
D、元素的非金属性越强,对应的氢化物还原性越弱.
解答 解:A、第ⅠA族元素除碱金属外还包括氢元素,故A错误;
B、氦最外层2个电子,但是0族,故B错误;
C、O、F无正价,故C错误;
D、元素的非金属性越强,对应的氢化物还原性越弱,第ⅦA元素从上到下,元素的非金属性逐渐减弱,其氢化物的还原性逐渐增强,故D正确;
故选D.
点评 本题考查元素周期表、周期律知识,为高频考点,侧重于学生的分析能力的考查,注意把握元素的性质的递变规律,难度不大.

练习册系列答案
相关题目
5.下列说法中不正确的是( )
| A. | 1mol酸与1mol碱发生中和反应时所释放的热量称为中和热 | |
| B. | 放热的反应在常温下不一定很容易发生 | |
| C. | 化学反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小 | |
| D. | 化学反应的本质是旧键的断裂和新键的形成 |
3.现有A、B、C三种金属,把A浸入C的盐溶液中,A的表面有C析出;把A、B用导线连接后同时浸入稀硫酸中,电子流动方向为:B→导线→A.A、B、C三种金属的活动性顺序为( )
| A. | B>A>C | B. | A>C>B | C. | A>B>C | D. | B>C>A |
10.如图是氢氧燃料电池结构示意图,下列关于该电池的说法中,正确的是( )
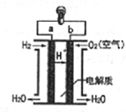

| A. | b极是负极 | B. | 正极发生氧化反应 | ||
| C. | a极的电极反应是H2-2e-=2H+ | D. | 该电池工作时,有淡蓝色火焰产生 |
7.下列有关化学反应原理的分析错误的是( )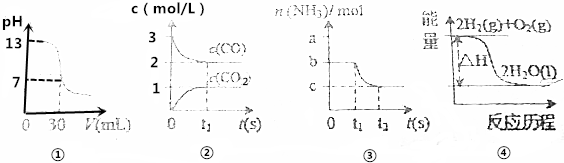
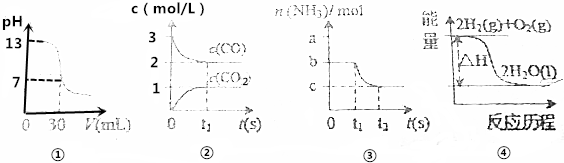
| A. | 图①表示25℃时,0.1000mol•L-1某一元酸滴定25.00mL 0.1000mol•L-1NaOH溶液,则根据图中数据可以计算出该温度下该一元酸的电离常数Ka | |
| B. | 图②表示某温度下的反应2CO(g)?C(s)+CO2(g)中的气体浓度随时间变化的曲线,则根据图中数据可计算该温度下的平衡常数K | |
| C. | 图③表示N2(g)+3H2(g)?2NH3(g)的平衡移动曲线,t1时刻改变的条件可能是降低压强 | |
| D. | 图④表示的反应热△H,可根据H2、O2、H2O的共价键的键能计算 |
4.含硒(Se)的保健品已开始进入市场.已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是( )
| A. | 非金属性比硫强 | B. | 阴离子比Br-半径小 | ||
| C. | 原子序数为34 | D. | 最高价氧化物的水化物显碱性 |
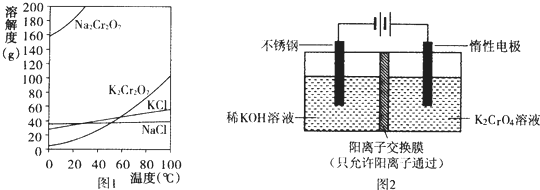
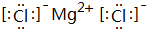 ,其中所含化学键的类型是离子键.
,其中所含化学键的类型是离子键.