题目内容
6.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+中的几种,请填写下列空白:①不做任何实验就可以肯定原溶液中不存在的离子是Cu2+、Fe3+
②取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量的稀硝酸,沉淀不消失.说明原溶液中,肯定存在的离子是Ag+
③取②中的滤液,加入过量的稀氨水,出现白色沉淀,说明原溶液中肯定有Mg2+.
分析 ①Cu2+、Fe3+均为有色离子;
②加入过量稀盐酸,有白色沉淀生成,再加入过量的稀硝酸,沉淀不消失,白色沉淀为AgCl;
③取②中的滤液,加入过量的稀氨水,出现白色沉淀,白色沉淀为氢氧化镁.
解答 解:①不做任何实验就可以肯定原溶液中不存在的离子是Cu2+、Fe3+,故答案为:Cu2+、Fe3+;
②加入过量稀盐酸,有白色沉淀生成,再加入过量的稀硝酸,沉淀不消失,白色沉淀为AgCl,说明原溶液中,肯定存在的离子是Ag+,故答案为:Ag+;
③取②中的滤液,加入过量的稀氨水,出现白色沉淀,白色沉淀为氢氧化镁,说明原溶液中,肯定存在的离子是Mg2+,故答案为:Mg2+.
点评 本题考查常见离子的检验,为高频考点,把握离子的性质、离子之间的反应为解答的关键,侧重分析与推断能力的考查,注意白色沉淀的判断,题目难度不大.

练习册系列答案
相关题目
2.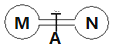 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | NH3 | HI | NO |
| 气体N | SO2 | HCl | Cl2 | O2 |
| A. | ③=④>①>② | B. | ③>④>①>② | C. | ④>③>②>① | D. | ④>③>①>② |
1.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,22.4LCO2含有的分子数为1NA | |
| B. | 常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA | |
| C. | 通常状况下,NA个CO2分子占有的体积约为22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
11.下列离子在溶液中不能大量共存的是( )
| A. | NH4+ K+ Ca2+ NO3- | B. | K+ Al3+ Br- NO3- | ||
| C. | Ba2+ K+ SO42- NO3- | D. | H+ K+ SO42- Cl- |




 .
.