题目内容
19.若50滴水正好是m mL,则1滴水所含的分子数是( )| A. | m×50×18×6.02×1023 | B. | $\frac{m×6.02×1{0}^{23}}{50×18}$ | ||
| C. | $\frac{18m×6.02×1{0}^{23}}{50}$ | D. | $\frac{50×18×m}{6.02×1{0}^{23}}$ |
分析 要求出1滴水所含的分子数,先要知道一个水分子的质量,再根据1mol水中所含的分子数和一个水分子的质量可求出1滴水所含的分子数.
解答 解:1滴水的体积$\frac{m}{50}$mL;则1滴水的质量=1g/ml×$\frac{m}{50}$mL=$\frac{m}{50}$g;
1mol水的质量为18g,1mol水中含有6.02×1023个水分子,设1滴水中水分子的个数为x,则$\frac{m}{50}$g:x=18g:6.02×1023,x=$\frac{m}{50×18}$×6.02×1023.
故选:B.
点评 本题考查以物质的量为核心计算公式,难度不大,侧重考查同学们利用物质的量进行计算的能力.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
20.14g铜、银合金与一定量某浓度的硝酸溶液反应,金属完全溶解,放出的气体与1.12L(标准状况下)氧气混合通入水中,恰好全部被水吸收,则合金中银的质量是( )
| A. | 2.7g | B. | 5.4g | C. | 8.1g | D. | 10.8g |
1.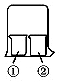 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )| ①中的物质 | ②中的物质 | 预测①的现象 | |
| A | 酚酞溶液 | 浓盐酸 | 无明显变化 |
| B | 饱和的KNO3溶液 | 浓硫酸 | 无明显变化 |
| C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
| D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
| A. | A | B. | B | C. | C | D. | D |
14.NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 60克SiO2含有2NA个Si-O共价键 | |
| B. | 实验室中用含4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA | |
| C. | 1L 0.2mol•L-1Al2(SO4)3溶液中的离子总数为NA | |
| D. | 标准状况下,22.4mLH2O约含有 3.73NA个原子 |
11.下列溶液中的Cl-浓度与150mL、1mol•L-1MgCl2溶液中的Cl-浓度相等的是( )
| A. | 300 mL、1mol•L-1NaCl溶液 | B. | 75 mL、2mol•L-1CaCl2溶液 | ||
| C. | 150 mL、2mol•L-1KCl溶液 | D. | 75 mL、1mol•L-1AlCl3溶液 |
9.一定能在下列溶液中大量共存的离子组是( )
| A. | 水电离产生的H+浓度为1×10-12mol•L-1的溶液:NH4+、Na+、Cl-、CO32- | |
| B. | 能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- | |
| C. | 0.1 mol/L的NaNO3溶液中:H+、Fe2+、Cl-、SO42- | |
| D. | 含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br- |