题目内容
11.下列溶液中的Cl-浓度与150mL、1mol•L-1MgCl2溶液中的Cl-浓度相等的是( )| A. | 300 mL、1mol•L-1NaCl溶液 | B. | 75 mL、2mol•L-1CaCl2溶液 | ||
| C. | 150 mL、2mol•L-1KCl溶液 | D. | 75 mL、1mol•L-1AlCl3溶液 |
分析 根据同一化学式中各微粒的浓度等于物质的物质的量浓度×离子个数,与溶液的体积无关,如150mL 1mol•L-1 MgCl2溶液中氯离子浓度为:n(Cl-)=1mol/L×2=2mol/L.
解答 解:150mL 1mol•L-1 MgCl2溶液中的Cl-的物质的量浓度为:c(Cl-)=2c(MgCl2)=2mol•L-1,
A.100mL 1mol•L-1 NaCl溶液中Cl-的物质的量浓度为:c(Cl-)=c(NaCl)=1mol•L-1,故A错误;
B.75mL 2mol•L-1CaCl2溶液中Cl-的物质的量浓度为:c(Cl-)=2c(CaCl2)=4mol•L-1,故B错误;
C.150mL 2mol•L-1 KCl溶液中Cl-的物质的量浓度为:c(Cl-)=c(KCl)=2mol•L-1,故C正确;
D.75mL 1mol•L-1AlCl3溶液中Cl-的物质的量浓度为:c(Cl-)=3c(AlCl3)=3mol•L-1,故D错误;
故选C.
点评 本题考查了物质的量浓度的计算,题目难度不大,试题侧重基础知识的考查,注意掌握物质的量浓度的概念及计算方法,明确物质的量浓度与溶液体积大小无关.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
12.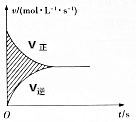 在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
 在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )| A. | X的浓度的变化量 | B. | Y的浓度的减小量 | ||
| C. | Z的物质的量的变化量 | D. | Y的物质的量的减小量 |
19.若50滴水正好是m mL,则1滴水所含的分子数是( )
| A. | m×50×18×6.02×1023 | B. | $\frac{m×6.02×1{0}^{23}}{50×18}$ | ||
| C. | $\frac{18m×6.02×1{0}^{23}}{50}$ | D. | $\frac{50×18×m}{6.02×1{0}^{23}}$ |
6.人类对赖以生存的地球环境的保护问题越来越重视,如何减少或取代高污染的化学品的使用,一直是许多化学家奋斗的目标,生产和应用绿色化工原料是达到该目标的最有效手段.碳酸二甲酯(简称DMC)是一种新化工原料,2008年在欧洲被誉为“非毒性化学品”.下列关于DMC的说法中正确的是( )
| A. | DMC的结构简式为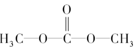 | |
| B. | DMC在空气不能燃烧 | |
| C. | DMC易溶于水,不溶于乙醇和丙酮 | |
| D. | DMC用于生产非毒性化工产品,故被誉为有机合成的“绿色化工原料” |
16.下列属于吸热反应的是( )
| A. | 锌粒与稀硫酸反应 | B. | 盐酸与氢氧化钠反应 | ||
| C. | 液化石油气的燃烧 | D. | 石灰石高温分解 |
3.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,22.4 L CO2中含有NA个CO2分子 | |
| B. | 1.7 g H2O2中含有的电子数为0.9NA | |
| C. | 标准状况下,2.24 L乙醇含有的分子数等于0.1NA | |
| D. | 分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
