题目内容
18.用NA表示阿伏伽德罗常数的值,下列叙述中不正确的是( )| A. | 28g乙烯和环丁烷的混合气体中含有的碳原子数为2NA | |
| B. | 常温常压下,46gNO2和N2O4的混合气体中含有的原子数为3NA | |
| C. | 标准状况下,22.4L水中含有的质子数为10NA | |
| D. | 1molNa与足量的O2反应,生成Na2O和Na2O2的混合物,转移电子数为NA |
分析 A、乙烯和环丁烷的最简式均为CH2;
B、NO2和N2O4的最简式均为NO2;
C、标况下水为液态;
D、钠和氧气反应后变为+1价.
解答 解:A、乙烯和环丁烷的最简式均为CH2,故28g混合物中含有的CH2的物质的量为2mol,则含2NA个碳原子,故A正确;
B、NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为1mol,则含3NA个原子,故B正确;
C、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量和质子数,故C错误;
D、钠和氧气反应后变为+1价,故1mol钠失去NA个电子,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
9.W、X、Y、Z均为短周期元素,W、X同主族,且W最高正价与最低负价的代数和为0,X、Y、Z的M层电子数分别为1,3,7.下列说法正确的是( )
| A. | 单质沸点:W>Y | |
| B. | X的最高价氧化物对应的水化物能与Y的氧化物反应 | |
| C. | W与X形成的化合物中含有共价键 | |
| D. | 简单离子的半径:X>Y>Z |
6.下列说法正确的是( )
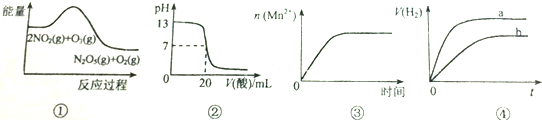

| A. | ①表示化学反应2NO2(g)+O3(g)═N2O5(g)+O2(g)△H>0 | |
| B. | ②表示25℃时,用0.5mol/LCH3COOH溶液滴定20mlNaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | ③表示10ml 0.01mol/L KMnO4 酸性溶液与过量的0.1mol/L H2C2O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | ④表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
13.下列说法正确的是( )
| A. | 任何酸与碱发生中和反应生成1mol H2O的过程中,能量变化均相同 | |
| B. | 已知:C (s,石墨)=C (s,金刚石)△H=+1.5 kJ•mol-1,则金刚石比石墨更稳定 | |
| C. | 若①2H2 (g)+O2 (g)=2H2O (g)△H=-a kJ•mol-1,②2H2 (g)+O2 (g)=2H2O (l)△H=-b kJ•mol-1,则 b>a | |
| D. | 能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
10.下列实验操作中,说法正确的是( )
| A. | 滴定管、移液管以及滴定过程中用于盛待测液的锥形瓶,使用前都需要洗涤与润洗 | |
| B. | 实验室制取氯气时,先装好二氧化锰,再检查装置的气密性 | |
| C. | 检验红色砖块中是否含三价铁的步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | |
| D. | 在中和热测定的实验中,将氢氧化钠溶液和盐酸混合反应后的最高温度作为末温度 |
7.下列化学反应中,不仅属于放热反应,而且属于中和反应的是( )
| A. | 澄清石灰水与稀硝酸反应 | B. | 硫在氧气中燃烧 | ||
| C. | 钠粒与稀盐酸反应 | D. | 碳酸氢钠溶液与氢氧化钠溶液反应 |
11.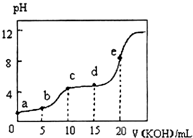 常温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1某二元弱酸H2R溶液,所得滴定曲线如图所示.下列叙述正确的是( )
常温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1某二元弱酸H2R溶液,所得滴定曲线如图所示.下列叙述正确的是( )
 常温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1某二元弱酸H2R溶液,所得滴定曲线如图所示.下列叙述正确的是( )
常温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1某二元弱酸H2R溶液,所得滴定曲线如图所示.下列叙述正确的是( )| A. | a点所示溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$<1012 | |
| B. | c点所示溶液中:c(K+)>c(HR-)>c(H2R)>c(R2-) | |
| C. | e点所示溶液中:c(H+)=c(HR-)+2c(H2R)+c(OH-) | |
| D. | 五个点中d点时c(HR-)最大 |