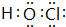题目内容
14.采用软锰矿浆(主要成分为Mn02,还含有Fe2O3、FeO、NiO、CoO等杂质)对工业烟气脱硫是工业生产中的一项新技术,该技术在脱硫的过程中还可以生产金属锰及化学肥料.该工艺流程如下图: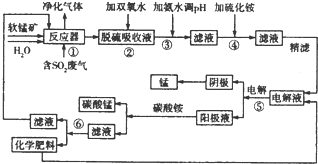
部分金属离子沉淀时的PH如下表:
| 阳离子 | Fe2+ | Fe3+ | Mn2+ | Ni2+ | Co2+ | |
| 氢氧化物沉淀 | 开始沉淀的PH | 7.5 | 2.2 | 8.8 | 6.4 | 9.0 |
| 完全沉淀的PH | 9.5 | 3.5 | 10.8 | 8.4 | ||
| 硫化物沉淀 | 开始沉淀的PH | 6.2 | 4.67 | |||
| 完全沉淀的PH | ||||||
(1)步骤①的反应器为“喷射鼓泡反应器,即将高速废气流通入到一定液固比的软锰矿浆中,并不断搅拌,采用这种设备的好处是增大二氧化硫与二氧化锰的接触面积,使其充分反应,从而提高反应速率,该反应的还原产物为亚铁离子、锰离子.
(2)写出步骤②中反应的离子方程式:2Fe2++2H++H2O2=2Fe3++2H2O
(3)若步骤③调节pH使用的是NaOH溶液,则导致的后果是后续得到有化学肥料中含有硫酸钠杂质.
(4)步骤④加入(NH4)2S的目的是除去溶液中的Ni2+、Co2+,加入(NH4)2S时溶液的pH最好控制在6.0以下,原因是防止锰离子生成硫化锰沉淀.
(5)步骤⑤所用设备名称为电解槽.
(6)步骤⑥的化学肥料为硫酸铵,该肥料加入到步骤⑤中的作用是增加溶液的导电性.
分析 二氧化硫与软锰矿浆作用生成硫酸锰和少量的硫酸铁、硫酸亚铁等,氧化环节:双氧水可将亚铁离子氧化为铁离子;加氨水调节溶液的PH把铁离子转化为沉淀除去;加硫化铵把重金属转化为沉淀除去;通过电解得到金属锰;在阳极液中加碳酸氢铵得碳酸锰和硫酸铵等,由此分析解答.
解答 解:二氧化硫与软锰矿浆作用生成硫酸锰和少量的硫酸铁、硫酸亚铁等,氧化环节:双氧水可将亚铁离子氧化为铁离子;加氨水调节溶液的PH把铁离子转化为沉淀除去;加硫化铵把重金属转化为沉淀除去;通过电解得到金属锰;在阳极液中加碳酸氢铵得碳酸锰和硫酸铵等,
(1)喷射鼓泡反应器,并不断搅拌,采用这种设备的好处是增大二氧化硫与二氧化锰的接触面积,使其充分反应,从而提高反应速率,缩短反应的时间,提高经济效益,锰由+4价变成+2价,铁离子还原成亚铁离子,故答案为:增大二氧化硫与二氧化锰的接触面积,使其充分反应,从而提高反应速率;亚铁离子、锰离子;
(2)亚铁离子被氧化成铁离子,反应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O,故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;
(3)若步骤③调节pH使用的是NaOH溶液,引入钠离子,则导致的后果是后续得到有化学肥料中含有硫酸钠,故答案为:后续得到有化学肥料中含有硫酸钠杂质;
(4)由表中的信息PH=6.2,锰离子开始沉淀,所以防止锰离子生成硫化锰沉淀,故答案为:防止锰离子生成硫化锰沉淀;
(5)步骤⑤所用是电解设备名称为电解槽,故答案为:电解槽;
(6)滤液中含有铵根离子和硫酸根离子,所以步骤⑥的化学肥料为硫酸铵,电解过程中加入硫酸铵是增加溶液的导电性,故答案为:硫酸铵;增加溶液的导电性.
点评 本题考查学生对元素及其化合物的主要性质的掌握、书写电极反应方程式、阅读题目获取新信息能力、对工艺流程的理解等,难度中等,需要学生具备扎实的基础与综合运用知识、信息分析解决问题能力.

①CaCl2液中通入CO2至过量
②澄淸石灰水通入SO2至过量
③氢氧化铁胶体中滴加稀硫酸至过量
④FeCl3溶液中逐滴加人氢氡化钠溶液至过量.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ④ |
| A. | 平衡前,随着反应的进行,容器内压强变小 | |
| B. | 平衡时,其他条件不变,分离出H2O(g),逆反应速率减小 | |
| C. | 平衡时,其他条件不变,升高温度平衡常数增大 | |
| D. | 其他条件不变,使用不同催化剂,HCl(g)的转化率不变 |
| 选项 | 有机酸X的数目 | 醇Y的数目 |
| A | 4种 | 3种 |
| B | 4种 | 2种 |
| C | 5种 | 3种 |
| D | 5种 | 2种 |
| A. | A | B. | B | C. | C | D. | D |
| 操作 | 现象 |
通入氯气至过量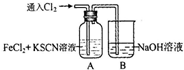 | Ⅰ、A中溶液变红 Ⅱ、稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是(用离子方程式表示)2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液.
甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
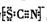 .
.①甲同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②通过实验证明了SCN- 中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成.
③若SCN-与Cl2反应生成1molCO2,则转移电子的物质的量是16mol.
| A. | 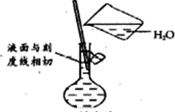 制溶液 | B. | 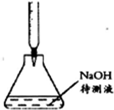 中和滴定 | ||
| C. | 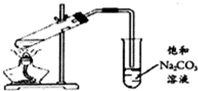 制备乙醇乙酯 | D. | 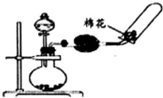 制备收集干燥的氨气 |
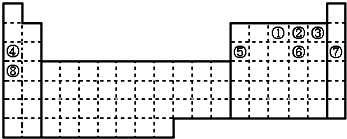
| A. | 铝的第一电离能比镁的第一电离能大 | |
| B. | 钾的第一电离能比镁的第一电离能大 | |
| C. | 在所有的元素中,F的第一电离能最大 | |
| D. | 第3周期所含元素中钠的第一电离能最小 |
| A. | 0.1a mol | B. | (0.1+a)mol | C. | (0.05+a)mol | D. | 2a mol |