题目内容
2.氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗.纯化工业级氧化锌(含Fe2+、Mn2+、Ni2+等杂质)的流程如图:
提示:在本实验条件下,Mn2+被氧化为MnO2;Ni2+不能被氧化;
高锰酸钾的还原产物是MnO2;反应④中产物的成分可能是ZnCO3•xZn(OH)2;
回答下列问题:
(1)反应②中除掉的杂质离子是Fe2+和Mn2+.
(2)反应③的反应类型为置换反应,过滤得到的滤渣中,除了过量的锌外还有镍(Ni).
(3)Mn2+发生反应的离子方程式为2MnO4-+3Mn2++2H2O=5MnO2↓+4H+,在加高锰酸钾溶液前,若pH较低,对除杂的影响是铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质.
(4)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是取最后一次少量水洗液于试管中,滴入1~2滴稀盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净.
(5)反应④中产物的成分可能是ZnCO3•xZn(OH)2,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x等于1.
分析 纯化工业级氧化锌和稀硫酸反应导致溶液中存在Fe2+、Mn2+、Zn2+和Ni2+,向浸出液中加入适量高锰酸钾溶液并调节溶液的pH约为5,Ni(Ⅱ)不能被氧化,Fe2+、Mn2+被氧化而被除去,同时溶液中有MnO2生成,过滤后,向滤液中加入Zn过滤,Zn和Ni2+发生氧化还原反应生成Ni,溶液中存在Zn2+,向滤液中加入碳酸钠溶液,生成ZnCO3•xZn(OH)2沉淀,煅烧碳酸锌沉淀生成ZnO,
(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+;
(2)反应③中加入Zn后,由于Zn比Ni活泼,可置换出Ni,以达到除Ni的目的;
(3)加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
(4)检验沉淀是否洗涤干净的方法是最后一次洗涤液,检验表面是否含有硫酸根离子;
(5)根据关系式ZnCO3•xZn(OH)2~(x+1)ZnO来计算.
解答 解:(1)纯化工业级氧化锌和稀硫酸反应导致溶液中存在Fe2+、Mn2+、Zn2+和Ni2+,向浸出液中加入适量高锰酸钾溶液并调节溶液的pH约为5,Ni(Ⅱ)不能被氧化,Fe2+、Mn2+被氧化而被除去,故答案为:Fe2+和Mn2+;
(2)反应③中加入Zn后,由于Zn比Ni活泼,可置换出Ni,以达到除Ni的目的,反应方程式为:Zn+Ni2+═Ni+Zn2+,此反应为置换反应,如果锌过量则在滤渣中会有多余的锌,
故答案为:置换反应; 镍(Ni);
(3)在本实验条件下,Mn2+被氧化为MnO2,反应②中除掉的杂质离子是Fe2+和Mn2+,发生的离子方程式为MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
故答案为:2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
(4)由于溶液中硫酸根离子属于杂质离子,因此可以检验测定洗涤液中是否存在硫酸根离子,操作为:取最后一次少量水洗液于试管中,滴入1~2滴稀盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净,
故答案为:取最后一次少量水洗液于试管中,滴入1~2滴稀盐酸,再滴入氯化钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净;
(5)ZnCO3•xZn(OH)2$\frac{\underline{\;高温\;}}{\;}$(x+1)ZnO+xH2O↑+CO2↑
125+99x (x+1)×81
11.2 8.1
$\frac{125+99x}{11.2}$=$\frac{(x+1)×81}{8.1}$,
x=1,
故答案为:1.
点评 本题综合考查混合物的分离和提纯,为高频考点,侧重考查学生分析问题、解答问题能力,明确流程图中各个步骤发生的反应及溶液中存在的微粒,知道常见离子的检验方法及实验现象,题目难度中等.

| A. | 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-5:10-7m之间 | |
| B. | 光线透过胶体时,胶体中可发生丁达尔效应 | |
| C. | Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 | |
| D. | 用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
| A. | 体积数据 | B. | 体积分数 | C. | 质量分数 | D. | 物质的量浓度 |
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④KClO3分解制取O2
⑤生石灰与水反应生成熟石灰
⑥CaCO3高温分解
⑦CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO
⑧Ba(OH)2•8H2O与固体NH4Cl混合
⑨C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2
⑩Al与盐酸反应.
| A. | ②④⑥⑦⑧⑨ | B. | ①②④⑥⑦⑧⑨ | C. | ①③④⑤⑥⑧⑩ | D. | ①②④⑧⑨ |
| A. | 化学平衡向正向移动,反应物浓度一定降低 | |
| B. | 化学平衡向正向移动,生成物的浓度一定增加 | |
| C. | 化学平衡向正向移动,反应物的转化率一定增大 | |
| D. | 化学平衡向正向移动时,正反应速率一定大于逆反应速率 |
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料.
①基态Ti2+中含有的电子数为20,电子占据的最高能级是3d,该能级具有的原子轨道数为5.
②BH4-中的B原子的杂化方式是sp3.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+<(填“>”“<”或“=”)H-.
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如表所示:
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)液氨是富氢物质,是氢能的理想载体.
①NH3的相对分子质量小于PH3,但NH3的沸点却远高于PH3,其原因是氨气分子之间可以形成氢键.
②NH3容易和分子中有空轨道的BF3反应形成新的化合物(用“→”表示配位键),该化合物的结构式为
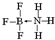 .
.(4)2008年,Yoon等人发现Ca与C60(分子结构如图甲)生成的Ca32C60能大量吸附H2分子.
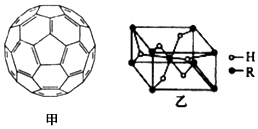
①C60晶体易溶于苯、CS2,C60是非极性(填“极性”或“非极性”)分子.
②1mol C60分子中,含有σ 键数目为90NA个.(阿伏加德罗常数数值为NA)
(5)某金属氢化物储氢材料的晶胞结构如图乙所示,该金属氢化物的化学式为H2R.已知该晶体的密度为a g•cm-3,金属元素R的相对原子质量为M,阿伏加德罗常数数值为NA,则该晶胞的体积为$\frac{2M+4}{{a{N_A}}}$cm3.
| A. | 纤维素在人体内可以水解成葡萄糖 | |
| B. | 组成蛋白质的元素中,一定含有碳、氢、氧、氮 | |
| C. | 适量摄入油脂,有助于人体吸收多种脂溶性维生素 | |
| D. | 天然蛋白质水解后的最终产物是a-氨基酸 |
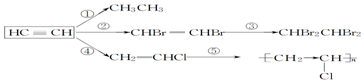
 ,加聚反应.
,加聚反应.