题目内容
9.与Li<Na<K<Rb<Cs的变化规律不符合的是( )| A. | 原子半径 | B. | 单质熔沸点 | ||
| C. | 与水或酸反应置换氢气的剧烈程度 | D. | 最高价氧化物对应水化物的碱性 |
分析 A.同主族从上到下原子半径逐渐增大;
B.碱金属元素中,随着原子序数的增大,金属的熔沸点逐渐降低;
C.碱金属元素中,随着原子序数的增大,金属的金属性逐渐增强;
D.碱金属元素中,随着原子序数的增大,金属的金属性逐渐增强,最高价氧化物对应水化物的碱性;
解答 解:A.第ⅠA族元素从上到下原子半径逐渐增大,与Li<Na<K<Rb<Cs的变化规律符合,故A正确;
B.碱金属元素中,随着原子序数的增大,金属的熔沸点逐渐降低,与Li<Na<K<Rb<Cs的变化规律不符合,故B错误;
C.碱金属元素中,随着原子序数的增大,金属的熔沸点逐渐降低,与水反应剧烈程度增强,与Li<Na<K<Rb<Cs的变化规律符合,故C正确;
D.碱金属元素中,随着原子序数的增大,金属的金属性逐渐增强,最高价氧化物对应水化物的碱性,与Li<Na<K<Rb<Cs的变化规律符合,故D正确;
故选:B.
点评 本题考查学生碱金属的性质递变规律,可以根据同主族元素性质的递变规律来回答,难度不大.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
20.下列化合物中只含有共价键的是( )
| A. | MgCl2 | B. | KCl | C. | NH4Cl | D. | H2SO4 |
17.高温下硫酸亚铁发生如下反应:2FeSO4=Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钙溶液中,得到的沉淀是( )
| A. | CaSO4和CaSO3 | B. | CaSO4 | C. | CaS | D. | CaSO3 |
4.下列化学用语正确的是( )
| A. | 二氧化碳分子的比例模型 | B. | NH3的电子式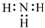 | ||
| C. | 乙烷的分子式 CH3CH3 | D. | 丙烯的结构简式 CH3CH=CH2 |
14.类比是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中,正确的是( )
| A. | IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| B. | CH4是正四面体结构,则SiH4也是正四面体结构 | |
| C. | 锂与氧气反应:4Li+O2═2 Li2O,则钠与氧气反应:4Na+O2═2Na2O | |
| D. | CaCO3与稀硝酸反应生成CO2,则CaSO3与稀硝酸反应生成SO2 |
1.把a、b、c、d 4块金属浸入稀硫酸中,用导线两两相连组成原电池.若把a、b相连时,a为负极;若a、c相连时,电流由c经导线流向a; b、d相连时,电子经由导线由d流向b,则四种金属的活动顺序由强到弱的顺序是( )
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>a>c>d |
18.家庭烹饪时,同时加酒和醋,烹饪出的菜更可口,这是因为有( )
| A. | 生成盐类物质 | B. | 生成酸类物质 | C. | 生成酯类物质 | D. | 生成醇类物质 |