题目内容
已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是( )
| 容器 | 实验1 | 实验2 | 实验3 |
| 反应物投入量(始态) | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度/mol?L-1 | cl | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强( Pa) | p1 | p 2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、a+b=92.4 |
| B、2cl>c3 |
| C、2p2<p3 |
| D、(α1+α3)<1 |
考点:化学平衡的计算,化学平衡的影响因素
专题:化学平衡专题
分析:甲容器反应物投入1molN2、3molH2,乙容器反应物投入量2molNH3,恒温且乙容器容积和甲容器相同,则甲容器与乙容器是等效平衡;
甲容器反应物投入1molN2、3molH2,丙容器反应物投入量4molNH3,采用极限转化法转化为反应物为2molN2、6molH2,是甲中的二倍,如果恒温且丙容器容积是甲容器2倍,则甲容器与丙容器也是等效平衡;所以丙所到达的平衡,可以看作在恒温且容积是甲容器两倍条件下,到达平衡后,再压缩体积为与甲容器体积相等所到达的平衡;据此分析平衡移动.
甲容器反应物投入1molN2、3molH2,丙容器反应物投入量4molNH3,采用极限转化法转化为反应物为2molN2、6molH2,是甲中的二倍,如果恒温且丙容器容积是甲容器2倍,则甲容器与丙容器也是等效平衡;所以丙所到达的平衡,可以看作在恒温且容积是甲容器两倍条件下,到达平衡后,再压缩体积为与甲容器体积相等所到达的平衡;据此分析平衡移动.
解答:
解:甲投入1molN2、3molH2,乙容器投入量2molNH3,恒温恒容条件下,甲容器与乙容器是等效平衡,各组分的物质的量、含量、转化率等完全相等;
而甲容器投入1molN2、3molH2,丙容器加入4molNH3,采用极限转化法丙相当于加入2molN2、6molH2,丙中加入量是甲中的二倍,如果恒温且丙容器容积是甲容器2倍,则甲容器与丙容器为等效平衡,所以丙所到达的平衡,可以看作在恒温且容积是甲容器两倍条件下,到达平衡后,再压缩体积为与甲容器体积相等所到达的平衡,由于该反应是体积减小的反应,缩小容器体积,增大了压强,平衡向着正向移动,所以丙中氮气、氢气转化率大于甲和乙的,
A、甲投入1molN2、3molH2,乙中投入2molNH3,则甲与乙是完全等效的,根据盖斯定律可知,甲与乙的反应的能量变化之和为92.4kJ,故a+b=92.4,故A正确;
B、丙容器反应物投入量4molNH3,采用极限转化法转化为反应物为2molN2、6molH2,是甲中的二倍,若平衡不移动,c3=2c1;丙相当于增大压强,平衡向着正向移动,所以丙中氨气的浓度大于乙中氨气浓度的二倍,即c3>2c1,故B错误;
C、丙容器反应物投入量4molNH3,是乙的二倍,若平衡不移动,丙中压强为乙的二倍;由于丙中相当于增大压强,平衡向着向着正向移动,所以丙中压强减小,小于乙的2倍,即2p2>p3,故C错误;
D、丙容器反应物投入量4molNH3,是乙的二倍,若平衡不移动,转化率α1+α3=1;由于丙中相当于增大压强,平衡向着向着正向移动,氨气的转化率减小,所以转化率α1+α3<1,故D正确;
故选AD.
而甲容器投入1molN2、3molH2,丙容器加入4molNH3,采用极限转化法丙相当于加入2molN2、6molH2,丙中加入量是甲中的二倍,如果恒温且丙容器容积是甲容器2倍,则甲容器与丙容器为等效平衡,所以丙所到达的平衡,可以看作在恒温且容积是甲容器两倍条件下,到达平衡后,再压缩体积为与甲容器体积相等所到达的平衡,由于该反应是体积减小的反应,缩小容器体积,增大了压强,平衡向着正向移动,所以丙中氮气、氢气转化率大于甲和乙的,
A、甲投入1molN2、3molH2,乙中投入2molNH3,则甲与乙是完全等效的,根据盖斯定律可知,甲与乙的反应的能量变化之和为92.4kJ,故a+b=92.4,故A正确;
B、丙容器反应物投入量4molNH3,采用极限转化法转化为反应物为2molN2、6molH2,是甲中的二倍,若平衡不移动,c3=2c1;丙相当于增大压强,平衡向着正向移动,所以丙中氨气的浓度大于乙中氨气浓度的二倍,即c3>2c1,故B错误;
C、丙容器反应物投入量4molNH3,是乙的二倍,若平衡不移动,丙中压强为乙的二倍;由于丙中相当于增大压强,平衡向着向着正向移动,所以丙中压强减小,小于乙的2倍,即2p2>p3,故C错误;
D、丙容器反应物投入量4molNH3,是乙的二倍,若平衡不移动,转化率α1+α3=1;由于丙中相当于增大压强,平衡向着向着正向移动,氨气的转化率减小,所以转化率α1+α3<1,故D正确;
故选AD.
点评:本题考查化学平衡影响因素、等效平衡、化学平衡的计算,题目计算量较大,题目难度较大,关键是构建平衡建立的等效途径,试题侧重对学生灵活运用基础知识解决实际问题的能力的培养.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
下列离子方程式中错误的是( )
| A、碳酸镁与H2SO4反应:MgCO3+2H+=Mg2++H2O+CO2↑ |
| B、向硝酸银溶液中加盐酸:Ag++Cl-=AgCl↓ |
| C、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、澄清石灰水与盐酸的反应:H++OH-=H2O |
下列物质属于电解质的是( )
| A、CO2 |
| B、浓硫酸 |
| C、蔗糖 |
| D、NaCl |
 某反应的反应过程中能量变化如图所示(图中E表示活化能),下列叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E表示活化能),下列叙述正确的是( )| A、逆反应的活化能大于正反应的活化能 |
| B、该反应为放热反应 |
| C、催化剂能改变反应的焓变 |
| D、催化剂能降低反应的活化能 |
下列除杂质(括号里物质为杂质)的方法正确的是 ( )
| A、乙酸乙酯(乙酸):加入NaOH溶液加热,分液 |
| B、苯(苯酚):溴水,过滤 |
| C、福尔马林(甲酸):加入Na2CO3溶液,分液 |
| D、苯(苯酚):加入NaOH溶液,分液 |
氢化钙(CaH2中H为-1价)可作为生氢剂,反应的化学方程式为CaH2+2H2O═Ca(OH)2+2H2↑.下列说法错误的是( )
| A、标准状况下生成1mol H2时转移2NA个电子 |
| B、CaH2是还原剂,H2O是氧化剂 |
| C、H2既是氧化产物又是还原产物 |
| D、氧化产物和还原产物的质量比是1:1 |
下列离子方程式正确的是( )
| A、Cl2与H2O反应:Cl2+H2O═2H++ClO-+Cl- |
| B、向Na2SiO3溶液中通入过量的CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- |
| C、向AlCl3溶液中滴加氨水至过量:Al3++3OH-═Al(OH)3↓ |
| D、将铜片投入浓硝酸中:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O |
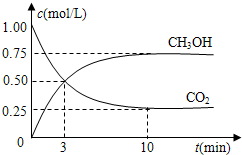 在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.
在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.