题目内容
下列除杂质(括号里物质为杂质)的方法正确的是 ( )
| A、乙酸乙酯(乙酸):加入NaOH溶液加热,分液 |
| B、苯(苯酚):溴水,过滤 |
| C、福尔马林(甲酸):加入Na2CO3溶液,分液 |
| D、苯(苯酚):加入NaOH溶液,分液 |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:A.乙酸乙酯与氢氧化钠反应;
B.溴以及三溴苯酚都溶于苯中;
C.甲醛以及甲酸钠都溶于水;
D.苯酚可与氢氧化钠溶液反应.
B.溴以及三溴苯酚都溶于苯中;
C.甲醛以及甲酸钠都溶于水;
D.苯酚可与氢氧化钠溶液反应.
解答:
解:A.乙酸乙酯与氢氧化钠反应,应用饱和碳酸钠溶液除杂,故A错误;
B.溴和苯酚反应生成三溴苯酚,三溴苯酚溶于苯中,应用氢氧化钠溶液除杂,故B错误;
C.甲醛以及甲酸钠都溶于水,应用蒸馏的方法分离,故C错误;
D.苯酚可与氢氧化钠溶液反应,可除去杂质,故D正确.
故选D.
B.溴和苯酚反应生成三溴苯酚,三溴苯酚溶于苯中,应用氢氧化钠溶液除杂,故B错误;
C.甲醛以及甲酸钠都溶于水,应用蒸馏的方法分离,故C错误;
D.苯酚可与氢氧化钠溶液反应,可除去杂质,故D正确.
故选D.
点评:本题考查物质的分离、提纯,侧重除杂的考查,把握物质的性质及选择合理的除杂方法为解答的关键,注意除杂不能引入新杂质,不能将原物质反应掉,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目
已知反应2SO2(g)+O2(g)?2SO3(g),下列判断正确的是( )
| A、2mol SO2和足量O2反应,必定生成2mol SO3 |
| B、该反应在容积不变的密闭容器中,若混合气的密度不变,说明达到平衡状态 |
| C、平衡时,SO2消耗速率必定等于O2生成速率的两倍 |
| D、平衡时,SO2浓度必定等于O2浓度的两倍 |
下列判断错误的是( )
| A、稳定性:H2O>H2S>H2Se |
| B、熔点:SiO2>NaCl>I2>CO2 |
| C、酸性:HCl>HBr>HI |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
现行的元素周期表的周期数和族数分别是( )
| A、7,18 | B、9,18 |
| C、7,16 | D、9,16 |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A、CO2的电子式是 |
| B、乙烯的结构简式是C2H4 |
C、Cl-的结构示意图 |
| D、K 原子的价层电子排布是1s22s22p63s23p64s1 |
已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是( )
| 容器 | 实验1 | 实验2 | 实验3 |
| 反应物投入量(始态) | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度/mol?L-1 | cl | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强( Pa) | p1 | p 2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、a+b=92.4 |
| B、2cl>c3 |
| C、2p2<p3 |
| D、(α1+α3)<1 |
科学家预言:“水不久将成为一个深刻的社会危机.”这是因为( )
| A、地球上水很少,不能满足人类的需要 |
| B、土地沙漠化,使空气中水蒸气不断减少 |
| C、由于地球表面气温的作用,水会被不断蒸发掉 |
| D、淡水资源不充足,分布又很不均匀,而且人类活动使水不断地受到污染,使淡水资源越来越紧缺 |
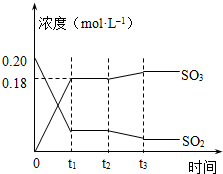 已知2SO2 (g)+O2(g)?2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如图所示:
已知2SO2 (g)+O2(g)?2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如图所示: