题目内容
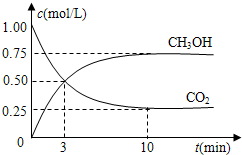 在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.
在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.(1)下列说法正确的是
A.进行到3分钟时,正反应速率和逆反应速率相等
B.10分钟后容器中各物质的物质的量不再改变
C.达到平衡后,再充入氩气反应速率不会改变
(2)求从反应开始到10min,氢气的平均反应速率v(H2)(写出计算过程).
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)根据图象给出的信息判断;
(2)由图可知,平衡时二氧化碳的浓度变化量为1mol/L-0.25mol/L=0.75mol/L,根据v=
计算v(CO2),再利用速率之比等于化学计量数之比计算v(H2)
(2)由图可知,平衡时二氧化碳的浓度变化量为1mol/L-0.25mol/L=0.75mol/L,根据v=
| △c |
| △t |
解答:
解:(1)A.正反应速率和逆反应速率相等,是指相同时间内,物质浓度变化量相同,而根据图象可知进行到3分钟时,CO2和CH3OH(g)的浓度相同,不能判断浓度变化量是否相同,故A错误;
B.10分钟后,CO2和CH3OH(g)的浓度不再变化,达到化学平衡状态,故B正确;
C.充入氩气,体积不变,各物质浓度不变,化学反应速率不变,故C正确;
故选BC;
(2)由图可知,10min到达平衡时二氧化碳的浓度变化量为1mol/L-0.25mol/L=0.75mol/L,所以v(CO2)=
=0.075mol/(L?min),
速率之比等于化学计量数之比,所以v(H2)=3v(CO2)=3×0.075mol/(L?min)=0.225mol/(L?min),
答:氢气的平均反应速率v(H2)=0.225mol/(L?min).
B.10分钟后,CO2和CH3OH(g)的浓度不再变化,达到化学平衡状态,故B正确;
C.充入氩气,体积不变,各物质浓度不变,化学反应速率不变,故C正确;
故选BC;
(2)由图可知,10min到达平衡时二氧化碳的浓度变化量为1mol/L-0.25mol/L=0.75mol/L,所以v(CO2)=
| 0.75mol/L |
| 10min |
速率之比等于化学计量数之比,所以v(H2)=3v(CO2)=3×0.075mol/(L?min)=0.225mol/(L?min),
答:氢气的平均反应速率v(H2)=0.225mol/(L?min).
点评:本题考查化学平衡的有关计算,催化剂对活化能和反应热的影响,本题难度不大,做题时注意平衡常数的计算和应用.

练习册系列答案
相关题目
室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- |
| B、水电离出的c(H+)=10-12mol/L的溶液中:K+、Na+、SO4 2-、AlO2- |
| C、能与铝反应生成氢气的溶液中:Mg2+、Na+、Cl-、NO3- |
| D、滴入KSCN显血红色的溶液中:NH4+、Mg2+、SO42-、Cl- |
已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是( )
| 容器 | 实验1 | 实验2 | 实验3 |
| 反应物投入量(始态) | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度/mol?L-1 | cl | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强( Pa) | p1 | p 2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、a+b=92.4 |
| B、2cl>c3 |
| C、2p2<p3 |
| D、(α1+α3)<1 |
下列说法不正确的是( )
| A、参加反应物质的性质是决定化学反应速率的主要因素 |
| B、光是影响某些化学反应速率的外界条件之一 |
| C、对于一个化学反应,既可以用反应物表示其化学反应速率,也可以用生成物表示其化学反应速率 |
| D、不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率 |