题目内容
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图.

请回答下列问题:
(1)在“图1”中,曲线 (填:a或b)表示使用了催化剂
(2)该反应在什么条件下有利于自发进行
A.高温 B.低温 C.任何温度
(3)下列说法正确的是
A.起始充入的CO为1mol B.增加CO浓度,CO的转化率增大
C.容器中气体平均相对分子质量保持不变时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2,再次达到平衡时
会减小
(4)从反应开始到建立平衡,氢气的平均反应速率为 ;该温度下CO(g)+2H2(g)?CH3OH(g)的化学平衡常数为.若体积保持不变再加入0.5mol CO和1mol CH3OH 则平衡向 方向移动.
(5)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P,且P1<P2).
(6)已知2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H=-385.8kJ/mol
又知H2O(l)=H2O(g)△H=+44kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 .

请回答下列问题:
(1)在“图1”中,曲线
(2)该反应在什么条件下有利于自发进行
A.高温 B.低温 C.任何温度
(3)下列说法正确的是
A.起始充入的CO为1mol B.增加CO浓度,CO的转化率增大
C.容器中气体平均相对分子质量保持不变时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2,再次达到平衡时
| n(CH3OH) |
| n(CO) |
(4)从反应开始到建立平衡,氢气的平均反应速率为
(5)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P,且P1<P2).
(6)已知2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H=-385.8kJ/mol
又知H2O(l)=H2O(g)△H=+44kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式
考点:物质的量或浓度随时间的变化曲线,反应热和焓变,热化学方程式,化学平衡的影响因素
专题:化学反应中的能量变化,化学平衡专题
分析:(1)根据图中反应的活化能的大小来分析是否使用催化剂;
(2)当△G=△H-T?△S<0时,反应能自发进行,据此判断;
(3)A、利用转化的CO和平衡时CO的量来分析;
B、增加CO浓度,会促进氢气的转化;
C、该反应为反应前后气体的物质的量不同,质量守恒;
D、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动;
(4)由图2计算用CO表示的反应速率,再利用反应速率之比等于化学计量数之比来计算氢气的反应速率;利用各物质平衡的浓度来计算化学平衡常数;通过计算比较Qc与K的大小关系来判断反应方向;
(5)根据温度和压强对该反应的影响来分析;
(6)根据盖斯定律结合已知热化学方程式来构建目标方程式来解答.
(2)当△G=△H-T?△S<0时,反应能自发进行,据此判断;
(3)A、利用转化的CO和平衡时CO的量来分析;
B、增加CO浓度,会促进氢气的转化;
C、该反应为反应前后气体的物质的量不同,质量守恒;
D、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动;
(4)由图2计算用CO表示的反应速率,再利用反应速率之比等于化学计量数之比来计算氢气的反应速率;利用各物质平衡的浓度来计算化学平衡常数;通过计算比较Qc与K的大小关系来判断反应方向;
(5)根据温度和压强对该反应的影响来分析;
(6)根据盖斯定律结合已知热化学方程式来构建目标方程式来解答.
解答:
解:(1)由图可知,曲线b降低了反应所需的活化能,则b使用了催化剂;
故答案为:b;
(2)当△G=△H-T?△S<0时,反应能自发进行,已知CO(g)+2H2(g)?CH3OH(g)该反应为熵减小的反应,即△S<0,且该反应中反应物的总能量大于生成物的总能量,则该反应为放热反应,即△H<0,若要△H-T?△S<0,则必须在高温条件下;
故答案为:A;
(3)A、由图2可知生成0.75mol/LCH3OH,则反应了0.75mol/LCO,平衡时有0.25mol/LCO,即CO的起始物质的量为(0.75mol/l+0.25mol/L)×2L=2mol,故A错误;
B、增加CO浓度,会促进氢气的转化,氢气的转化率增大,但CO的转化率减小,故B错误;
C、该反应为反应前后气体的物质的量不同,质量守恒,所以气体平均相对分子质量逐渐增大,当气体平均相对分子质量保持不变时,反应已达平衡状态,故C正确;
D、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动,再次达到平衡时
会增大,故D错误;
故答案为:C;
(4)由图2可知,反应中减小的CO的浓度为1mol/L-0.25mol/L=0.75mol/L,10min时达到平衡,
则用CO表示的化学反应速率为
=0.075mol?L-1?min-1,
因反应速率之比等于化学计量数之比,则v(H2)=0.075mol?L-1?min-1×2=0.15mol?L-1?min-1,
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
开始:1mol/L 2mol/L 0
转化:0.75mol/L 1.5mol/L 0.75mol/L
平衡:0.25mol/L 0.5mol/L 0.75mol/L
则化学平衡常数K=
=
=12 L2?mol-2;
若体积保持不变再加入0.5mol CO和1mol CH3OH,则Qc=
=
=10<K,反应未达到平衡状态,则反应向正反应方向进行;
故答案为:0.15mol?L-1?min-1;12 L2?mol-2;正反应;
(5)CO(g)+2H2(g) CH3OH(g)△H<0,则温度越高,逆向反应进行的程度越大,甲醇的含量就越低,压强增大,反应正向进行的程度大,则甲醇的含量高,则图象为:
CH3OH(g)△H<0,则温度越高,逆向反应进行的程度越大,甲醇的含量就越低,压强增大,反应正向进行的程度大,则甲醇的含量高,则图象为:
 ;
;
故答案为: ;
;
(5)32g的CH3OH(g)的物质的量为1mol,
已知:CH3OH(g)+
O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol ①
H2O(l)=H2O(g)△H=+44kJ/mol ②
根据盖斯定律①-②×2得:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-280.9kJ/mol,
故答案为:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-280.9kJ/mol.
故答案为:b;
(2)当△G=△H-T?△S<0时,反应能自发进行,已知CO(g)+2H2(g)?CH3OH(g)该反应为熵减小的反应,即△S<0,且该反应中反应物的总能量大于生成物的总能量,则该反应为放热反应,即△H<0,若要△H-T?△S<0,则必须在高温条件下;
故答案为:A;
(3)A、由图2可知生成0.75mol/LCH3OH,则反应了0.75mol/LCO,平衡时有0.25mol/LCO,即CO的起始物质的量为(0.75mol/l+0.25mol/L)×2L=2mol,故A错误;
B、增加CO浓度,会促进氢气的转化,氢气的转化率增大,但CO的转化率减小,故B错误;
C、该反应为反应前后气体的物质的量不同,质量守恒,所以气体平均相对分子质量逐渐增大,当气体平均相对分子质量保持不变时,反应已达平衡状态,故C正确;
D、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动,再次达到平衡时
| n(CH3OH) |
| n(CO) |
故答案为:C;
(4)由图2可知,反应中减小的CO的浓度为1mol/L-0.25mol/L=0.75mol/L,10min时达到平衡,
则用CO表示的化学反应速率为
| 0.75mol/L |
| 10min |
因反应速率之比等于化学计量数之比,则v(H2)=0.075mol?L-1?min-1×2=0.15mol?L-1?min-1,
CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)开始:1mol/L 2mol/L 0
转化:0.75mol/L 1.5mol/L 0.75mol/L
平衡:0.25mol/L 0.5mol/L 0.75mol/L
则化学平衡常数K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.75mol/L |
| 0.25mol/L×(0.5mol/L )2 |
若体积保持不变再加入0.5mol CO和1mol CH3OH,则Qc=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.75+0.5 |
| (0.25+0.25)×0.52 |
故答案为:0.15mol?L-1?min-1;12 L2?mol-2;正反应;
(5)CO(g)+2H2(g)
 CH3OH(g)△H<0,则温度越高,逆向反应进行的程度越大,甲醇的含量就越低,压强增大,反应正向进行的程度大,则甲醇的含量高,则图象为:
CH3OH(g)△H<0,则温度越高,逆向反应进行的程度越大,甲醇的含量就越低,压强增大,反应正向进行的程度大,则甲醇的含量高,则图象为: ;
;故答案为:
 ;
;(5)32g的CH3OH(g)的物质的量为1mol,
已知:CH3OH(g)+
| 3 |
| 2 |
H2O(l)=H2O(g)△H=+44kJ/mol ②
根据盖斯定律①-②×2得:CH3OH(g)+
| 3 |
| 2 |
故答案为:CH3OH(g)+
| 3 |
| 2 |
点评:本题考查化学反应速率、化学平衡及能量变化等,学生应注意图象的利用来分析解决问题,图象中的信息是解答本题的关键,题目综合性强,难度中等.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是( )
| 容器 | 实验1 | 实验2 | 实验3 |
| 反应物投入量(始态) | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度/mol?L-1 | cl | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强( Pa) | p1 | p 2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、a+b=92.4 |
| B、2cl>c3 |
| C、2p2<p3 |
| D、(α1+α3)<1 |
晨的树林,可以观测到一束束的阳光透过树叶,射入林间,这是种现象源自胶体的( )
| A、丁达尔效应 | B、聚沉 |
| C、电泳 | D、折射 |


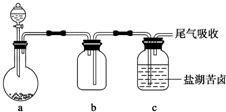
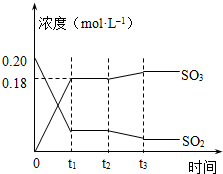 已知2SO2 (g)+O2(g)?2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如图所示:
已知2SO2 (g)+O2(g)?2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如图所示: