题目内容
16.(1)实验室中制备溴酸盐过程如下: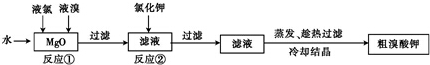
根据上述转化关系回答下列问题:
反应①的化学方程式为6MgO+Br2+5Cl2=Mg(BrO3)2+5MgCl2.
(2)已知在酸性条件下溴酸盐可发生如下离子反应:
I.2BrO3-+10Cl-+12H+═5Cl2↑+Br2+6H2O
Ⅱ.6BrO3-+5Cl-+6H+═5ClO3-+3Br2+3H2O
Ⅲ.BrO3-+5Br-+6H+═3Br2+3H2O
①上述反应所涉及的粒子中,氧化性最强的是BrO3-.
②在KCl和KBr的酸性混合溶液中,加人过量的KBrO3其氧化产物为KClO3、Br2,还原产物为Br2.
③将12mL0.4mol•L-1KBrO3溶液和10mL0.6mol•L-1KCl溶液在稀H2SO4中混合,充分反应后产物KClO3和Cl2的物质的量之比为3:1.
分析 (1)由于反应②中只加入KCl,不会发生氧化还原反应,反推知反应①中必生成BrO3-,由此得反应①中MgOH和氯气、溴反应生成溴酸镁和氯化镁;
(2)①同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
②可知KBrO3过量时,Cl-被氧化成ClO3-,还原产物为Br2,反应Ⅲ中Br2既是氧化产物也是还原产物;
③n(KBrO3)=0.4mol/L×0.012L=4.8×10-3 mol,n(KCl)=0.6mol/L×0.01L=6×10-3 mol,两者物质的量之比为4:5,
设参加反应Ⅰ的KBrO3的物质的量为x,则参加反应Ⅱ的KBrO3的物质的量为(4-x),再结合Cl原子守恒计算.
解答 解:(1)由于反应②中只加入KCl,不会发生氧化还原反应,反推知反应①中必生成BrO3-,由此得反应①中的化学方程式为6MgO+Br2+5Cl2=Mg(BrO3)2+5MgCl2,
故答案为:6MgO+Br2+5Cl2=Mg(BrO3)2+5MgCl2;
(2)①在三个反应中BrO3-均作氧化剂,所以氧化性其最强,
故答案为:BrO3-;
②对比反应Ⅰ和Ⅱ,可知KBrO3过量时,Cl-被氧化成ClO3-,还原产物为Br2,反应Ⅲ中Br2既是氧化产物也是还原产物,所以加人过量的KBrO3其氧化产物是KClO3、Br2,还原产物是Br2,
故答案为:KClO3、Br2;Br2;
③n(KBrO3)=0.4mol/L×0.012L=4.8×10-3 mol,n(KCl)=0.6mol/L×0.01L=6×10-3 mol,两者物质的量之比为4:5,设参加反应Ⅰ的KBrO3的物质的量为x,则参加反应Ⅱ的KBrO3的物质的量为(4-x),由Cl-守恒得:5x+$\frac{5}{6}$(4-x)=5,得x=$\frac{2}{5}$,反应Ⅰ生成的氯气为1,反应Ⅱ生成的KClO3为3,
则充分反应后产物KClO3和Cl2的物质的量之比为3:1,
故答案为:3:1.
点评 本题考查物质制备,为高频考点,侧重考查氧化还原反应及其有关计算,明确物质的性质、物质之间转化、氧化还原反应基本原理及原子守恒是解本题关键,题目难度中等.

 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1Na2CO3溶液与0.1 mol•L-1NaHCO3溶液等体积混合:$\frac{3}{2}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1Na2C2O4溶液与0.1 mol•L-1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O42-)+c(OH-)=c(Na+)+c(H+) |
| A. | 食醋的主要成分是醋酸,它是一种弱酸 | |
| B. | 苯酚有毒,但可用于杀菌消毒 | |
| C. | 聚乙烯塑料制品可用于食品的包装 | |
| D. | 福尔马林可作食品的保鲜剂 |
| A. | 盐酸的导电能力一定大于醋酸 | |
| B. | 在氨水中加入无水醋酸,溶液的导电能力基本不变 | |
| C. | 在氢氧化钡的稀溶液中,c(OH-)=2c(Ba2+) | |
| D. | 在磷酸的稀溶液中,c(H+)=3c(PO43-) |
| A. | CH3COOH | B. | CH3CH2CHO | ||
| C. | CH3CH=CHCH2CH2CH3 | D. | CH3CH2CH2CH2CH3 |
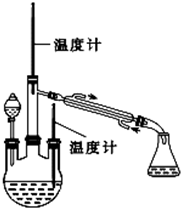 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).