��Ŀ����
17��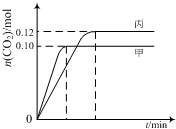 һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��2NO��g��+2CO��g��?N2��g��+2CO2��g��
һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��2NO��g��+2CO��g��?N2��g��+2CO2��g������������ʼ���ʵ����뷴Ӧ�¶����±���ʾ����Ӧ�����мס���������CO2�����ʵ�����ʱ��仯��ϵ����ͼ��ʾ��
| ���� | �¶�/�� | ��ʼ���ʵ���/mol | |
| NO ��g�� | CO ��g�� | ||
| �� | T1 | 0.20 | 0.20 |
| �� | T1 | 0.30 | 0.30 |
| �� | T2 | 0.20 | 0.20 |
| A�� | �÷�Ӧ������ӦΪ���ȷ�Ӧ | |
| B�� | �ﵽƽ��ʱ������CO2����������ȼ��е�С | |
| C�� | T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2����Ӧ�ﵽ��ƽ��ǰv��������v���棩 | |
| D�� | T2��ʱ������ʼʱ����г���0.06mol N2��0.12 mol CO2�����ƽ��ʱN2��ת���ʴ���40% |
���� A���ȹ���ƽ�¶ȸߣ���ƽ��״̬������̼���ʵ���С��˵���¶�Խ��ƽ��������У�
B�����п��Կ����Ǽ���ʼ���ﵽƽ��״̬���ټ���0.1molNO��0.1molCO���൱������ƽ��ѹǿ��ƽ��������У�
C����״̬��ƽ��ʱCO���ʵ���Ϊ0.10mol��������м������ƽ�ⳣ����������ʼ������Ũ���̺�ƽ�ⳣ���Ƚ��жϷ�Ӧ���з���
D��T2��ʱ������ͼ���֪ƽ��״̬��CO���ʵ���Ϊ0.12mol������ʼʱ����г���0.06mol N2��0.12 mol CO2����Ӧ������еõ�ƽ��״̬������ʼ��Ϊ0.12molNO��0.12molCO�ﵽ��ƽ����Ƚϣ�����ʼ��0.2molCO��NO��ȣ��൱�ڼ�����NO��CO0.08mol��CO��NO��ѹǿ��Сƽ��������У�
��� �⣺A.2NO��g��+2CO��g��?N2��g��+2CO2��g�����ȹ���ƽ�¶ȸߣ���״̬�¶ȸ��ڱ���T1��T2����ʱ��ƽ��״̬������̼���ʵ���С��˵���¶�Խ��ƽ��������У��淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ����A����
B�����п��Կ����Ǽ���ʼ���ﵽƽ��״̬���ټ���0.1molNO��0.1molCO���൱������ƽ��ѹǿ��ƽ��������У��ﵽƽ��ʱ������CO2����������ȼ��еĴ�B����
C����״̬��ƽ��ʱCO���ʵ���Ϊ0.10mol��������м������ƽ�ⳣ����
2NO��g��+2CO��g��?N2��g��+2CO2��g��
��ʼ����mol/L�� 0.1 0.1 0 0
�仯����mol/L�� 0.05 0.05 0.025 0.05
ƽ������mol/L�� 0.05 0.05 0.025 0.05
K=$\frac{0.0{5}^{2}��0.025}{0.0{5}^{2}��0.0{5}^{2}}$=10��
T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2��Qc=$\frac{\frac{0.4}{2}����\frac{0.4}{2}��^{2}}{��\frac{0.4}{2}��^{2}����\frac{0.4}{2}��^{2}}$=5��K=10����Ӧ�ﵽ��ƽ��ǰv��������v���棩����C����
D��T2��ʱ��ƽ��״̬CO���ʵ���Ϊ0.12mol��
2NO��g��+2CO��g��?N2��g��+2CO2��g��
��ʼ����mol�� 0.2 0.2 0 0
ת������mol�� 0 0 0.1 0.2
�仯����mol�� 0.08 0.08 0.04 0.08
ƽ������mol�� 0.12 0.12 0.04 0.08
2NO��g��+2CO��g��?N2��g��+2CO2��g��
��ʼ����mol�� 0 0 0.06 0.12
ת���� 0.12 0.12 0 0
����ʼʱ����г���0.06mol N2��0.12 mol CO2����Ӧ������еõ�ƽ��״̬������ʼ��Ϊ0.12molNO��0.12molCO�ﵽ��ƽ����ͬ������ʼ��0.2molCO��NO��ȣ��൱�ڼ�����NO��CO0.08mol��CO��NO��ѹǿ��Сƽ��������У����Ե���ת���ʴ���40%����D��ȷ��
��ѡD��
���� ���⿼���˻�ѧƽ��Ӱ�����أ����ݷ����жϣ���Ҫ��ƽ�ⳣ���ļ����ͼ�ߵ�����Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д� â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�I����ʵ������ģ�ҵ�������̿���Ҫ�ɷ�ΪMnO2��������SiO2��Fe2O3��A12O3�ȣ��Ʊ������̵����ʣ����������ͼ��
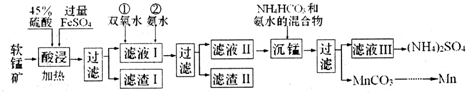
��֪��̼�����ڿ����и��¼��ȹ������ΪMn2O3���������������Ksp������ֵ�������
| ���� | Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Al��OH��3 |
| Ksp | 10-13 | 10-17 | 10-39 | 10-33 |
��2������ҺI �еμ�˫��ˮ��Ŀ���ǽ�Fe2+����ΪFe3+������ת��ΪFe��OH��3��ȥ�������ҺI ��c��Mn2+��=0.1mol•L-1��Ϊ��֤�μӰ�ˮ������Mn��OH��2��Ӧ������ҺpH���Ϊ8��
��3�������̡������е����ӷ���ʽΪMn2++HCO3-+NH3•H2O=MnCO3��+NH4++H2O��
��4����̼���̺ͽ�����Ϊԭ�Ͽ����Ʊ����̣�д���Ʊ����������һ����Ӧ�Ļ�ѧ����ʽMn2O3+2Al$\frac{\underline{\;����\;}}{\;}$Al2O3+2Mn��
��ѧ�ҷ�����NH3ȼ�ϵ�أ���KOHΪ����ʣ�ԭ����ͼ��ʾ��
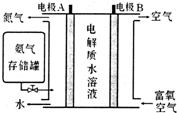
��5����ȼ�ϵ�صĸ�����ӦʽΪ2NH3+6OH--6e-=N2+6H2O��
��6���Ըõ��Ϊ��Դ����ʯī�缫�������أ�K2MnO4����Һ��ȡ������أ�ͨ��10���ӣ�����ǿ��Ϊ0.5A�������Ƶø������0.49g����֪1mol������������Ϊ96500C����
| A�� | 1mol����1molCl2��ַ�Ӧ��ת�Ƶ�����Ϊ3NA | |
| B�� | ���³�ѹ�£�2gD216O �к������������������������������ | |
| C�� | 14g ����ʽΪCnH2n �ģ�n��2�������к��е�C=C ����Ŀһ��Ϊ$\frac{{N}_{A}}{n}$ | |
| D�� | �ں�Al3+����ΪNA��AlCl3��Һ�У�Cl-����Ϊ3NA |
| A�� | MgSO4��Һ��Ba��OH��2��Һ��ϣ�Ba2++SO42-=BaSO4�� | |
| B�� | 0.3 mol FeBr2��0.4 mol Cl2����Һ�з�Ӧ��8Cl2+6Fe2++10Br-=6Fe3++16Cl-+5Br2 | |
| C�� | Cu��ϡHNO3��Ӧ��Cu+4H++2NO3-=Cu2++2NO��+2H2O | |
| D�� | AgCl��������������ˮ��Ag++2NH3•H2O=[Ag��NH3��2]++2H2O |
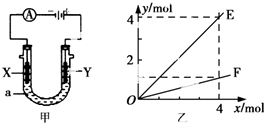
| A�� | ����װ�����ڵ�⾫��ͭ����XΪ��ͭ��YΪ��ͭ��������Һa����������ͭ���Ȼ�ͭ��Һ | |
| B�� | ��ͼ��װ���ö��Ե缫���AgN03��Һ����ͼ�Һ�����x��ʾ����缫�ĵ��ӵ����ʵ�������E�ɱ�ʾ��Ӧ������������ʵ�����F��ʾ���������������ʵ��� | |
| C�� | ��ͼ��װ���ö��Ե缫���һ��Ũ�ȵ�����ͭ��Һ��ͨ��һ��ʱ�����0.5mol��̼��ͭ�պûָ���ͨ��ǰ��Ũ�Ⱥ�pH�����������ת�Ƶĵ���Ϊ2.0 mol | |
| D�� | ��X��YΪ���缫��a��ҺΪ500 mL KCl��KNO3�Ļ��Һ������һ��ʱ����������õ���״����11.2 L���壬��ԭ���Һ��KCl�����ʵ���Ũ������Ϊ2.0 molL-1 |
| A�� | ����Һ�У�H+��Mg2+��NO3-��Cl-���Դ������� | |
| B�� | ����Һ��ʹ���۵⻯����ֽ��������Ӧ�����ӷ���ʽΪ��Fe3++2I-�TFe2++I2 | |
| C�� | ����Һ������Ba��OH��2��Һ��Ӧ�����ӷ���ʽΪ��Fe3++SO42-+Ba2++3OH-�TFe��OH��3��+BaSO4�� | |
| D�� | ����Һ������ͭ�۷�Ӧ�����ӷ���ʽΪ��3Cu+2Fe3+�T2Fe+3Cu2+ |
����A ��B ��C ��D ��E ��F ��G ��ƿ��ͬ���ʵ���Һ�����Ǹ���Na2CO3 ��NaSO4 ��KCl ��AgNO3 ��MgC12 ��Cu(NO3����Ba(OH��2��Һ��һ�֡�Ϊ�˼��𣬸�ȡ������Һ����������ϣ�ʵ�������±���ʾ�����С�������ʾ���ɳ����������һ����ʾ�۲첻�����Ա仯��
A | B | C | D | E | F | G | |
A | - | - | - | - | - | - | �� |
B | - | - | - | - | - | �� | �� |
C | - | - | - | �� | - | �� | �� |
D | - | - | �� | - | �� | �� | �� |
E | - | - | - | �� | - | �� | - |
F | - | �� | �� | �� | �� | - | �� |
G | �� | �� | �� | �� | - | �� | - |
��д���й����ʵĻ�ѧʽ��A:__________,C:__________,E:___________,G:___________��
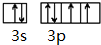 ����Ԫ�صķ�����S��
����Ԫ�صķ�����S��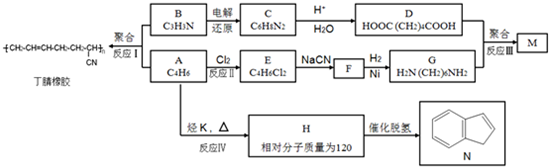
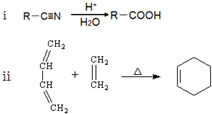
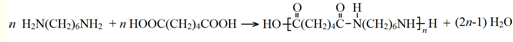 ��
�� ��
��