题目内容
9.下列说法错误的是( )| A. | 在共价化合物中不可能含有离子键 | |
| B. | 阴阳离子之间通过静电作用力形成的化学键,叫离子键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 离子化合物中不一定含有金属元素 |
分析 A.含离子键的化合物一定为离子化合物;
B.阴阳离子之间以静电作用成键;
C.离子化合物中可以含共价键;
D.非金属元素之间也能形成离子键.
解答 解:A.含离子键的化合物一定为离子化合物,则在共价化合物中不可能含有离子键,故A正确;
B.阴阳离子之间以静电作用成键,则阴阳离子之间通过静电作用力形成的化学键,叫离子键,故B正确;
C.离子化合物中可以含共价键,如NaOH中含共价键,为离子化合物,故C错误;
D.非金属元素之间也能形成离子键,如铵盐是由非金属元素形成的离子化合物,故D正确;
故选C.
点评 本题考查化学键和化合物的类型,注意离子键、共价键与化合物的关系,学会利用实例分析解答,题目难度不大.

练习册系列答案
相关题目
19.下表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题.
(1)地壳中含量最多的元素是O;
(2)N和O中,原子半径较小的是O;
(3)单质的化学性质最不活泼的是Ar;
(4)S原子结构示意图是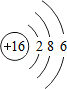 ;
;
(5)HF和HCl中,热稳定性较强的是HF;
(6)SiO2常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(7)元素最高价氧化物对应的水化物中,具有两性的是Al2O3(填化学式),碱性最强的是NaOH(填化学式);
(8)新制氯水有漂白作用,是因为其中含有HClO(填“HCl”或“HCIO”);
(9)碳元素的最高价氧化物的化学式是CO2,其碳元素与氧元素的物质的量比n(C):n(O)=1:2.
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
(2)N和O中,原子半径较小的是O;
(3)单质的化学性质最不活泼的是Ar;
(4)S原子结构示意图是
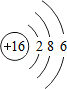 ;
;(5)HF和HCl中,热稳定性较强的是HF;
(6)SiO2常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(7)元素最高价氧化物对应的水化物中,具有两性的是Al2O3(填化学式),碱性最强的是NaOH(填化学式);
(8)新制氯水有漂白作用,是因为其中含有HClO(填“HCl”或“HCIO”);
(9)碳元素的最高价氧化物的化学式是CO2,其碳元素与氧元素的物质的量比n(C):n(O)=1:2.
4.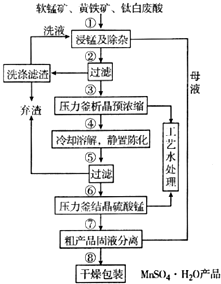 随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题:
随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题:
(1)实验室在过滤操作过程中,使用的玻璃仪器名称为烧杯、玻璃棒、漏斗.
(2)“浸锰”反应中往往有副产物MnS2O6的生成.温度对“浸锰”反应的影响如图1、图2所示,为减少MnS2O6的生成,“浸锰”的适宜温度为150℃(或150℃以上). (3)经查阅资料,生成相应氢氧化物时的pH如表所示.
(3)经查阅资料,生成相应氢氧化物时的pH如表所示.
实际生产过程中,①中加入一定量纯MnO2粉末的主要作用是将Fe2+氧化为Fe3+,将过量的SO2氧化除去;②中调节pH为3.5时,沉淀的主要成分是Fe(OH)3.
(4)⑤中所得的滤液中含有Cu2+,可添加过量的难溶电解质MnS除去Cu2+,经过滤,得到纯净的MnSO4.用平衡移动原理解释加入MnS的作用:MnS存在沉淀溶解平衡,MnS(S)?Mn2+(aq)+S2-(aq),加入后铜离子和硫离子结合市场难溶的硫化铜沉淀,S2-(aq)+Cu2+(aq)?CuS(S)生成的CuS比MnS更难溶,促进MnS不断溶解,平衡右移,使Cu2+除去.
(5)检验⑥中沉淀是否洗涤干净的方法是取少量最后一次洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净;反之则未洗干净.
 随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题:
随着科学技术的不断进步,锰的用量和应用领域不断扩大.硫酸锰作为基础锰盐,研究、开发生产硫酸锰的新工艺,尤其必要.现代工业常以软锰矿(主要成分为MnO2,杂质为铁和铜的化合物等)为原料通过“浸锰”操作制备高纯硫酸锰,工艺流程示意图如图所示,请回答下列问题:(1)实验室在过滤操作过程中,使用的玻璃仪器名称为烧杯、玻璃棒、漏斗.
(2)“浸锰”反应中往往有副产物MnS2O6的生成.温度对“浸锰”反应的影响如图1、图2所示,为减少MnS2O6的生成,“浸锰”的适宜温度为150℃(或150℃以上).
 (3)经查阅资料,生成相应氢氧化物时的pH如表所示.
(3)经查阅资料,生成相应氢氧化物时的pH如表所示.| 化学式 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
(4)⑤中所得的滤液中含有Cu2+,可添加过量的难溶电解质MnS除去Cu2+,经过滤,得到纯净的MnSO4.用平衡移动原理解释加入MnS的作用:MnS存在沉淀溶解平衡,MnS(S)?Mn2+(aq)+S2-(aq),加入后铜离子和硫离子结合市场难溶的硫化铜沉淀,S2-(aq)+Cu2+(aq)?CuS(S)生成的CuS比MnS更难溶,促进MnS不断溶解,平衡右移,使Cu2+除去.
(5)检验⑥中沉淀是否洗涤干净的方法是取少量最后一次洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净;反之则未洗干净.
1.下列说法中不正确的是( )
| A. | 液化石油气、汽油、柴油和润滑油的主要成分都是碳氢化合物 | |
| B. | 可以通过灼烧时的特殊气味来鉴别蛋白质 | |
| C. | 用溴水既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯 | |
| D. | 乙烯、氯乙烯和聚氯乙烯都能因发生加成反应而使溴水褪色 |
18.化学反应经常伴随着颜色变化,下列有关反应获得的颜色不正确的是( )
| A. | 蛋白质遇浓硝酸呈现黄色 | |
| B. | 淀粉溶液遇单质碘呈现蓝色 | |
| C. | 苯酚显弱酸性,其溶液可以使石蕊试液变红色 | |
| D. | 苯酚在空气中氧化呈现粉红色 |
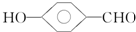 的沸点比
的沸点比 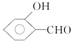 高,原因是
高,原因是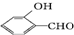 形成分子内氢键,而
形成分子内氢键,而 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.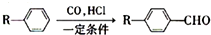 为合成某种液晶材料的中间体M,有人提出如下不同的合成途径
为合成某种液晶材料的中间体M,有人提出如下不同的合成途径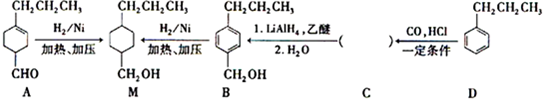
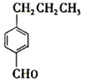 ,由C→B反应类型为加成反应.
,由C→B反应类型为加成反应.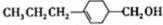 和
和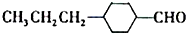 (写结构简式)两种互为同分异构体杂质生成.
(写结构简式)两种互为同分异构体杂质生成.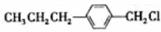 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$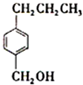 +NaCl;
+NaCl; .
.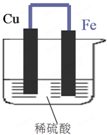 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.