题目内容
19.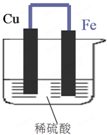 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.(1)铁片为负极,其电极反应式Fe-2e-=Fe2+.
(2)铜片上的现象是有大量气泡产生,其发生的反应的类型是还原反应.(填“氧化”或“还原”)
(3)若导线中通过了0.6mol电子,Fe的质量理论上减少16.8克.
分析 该原电池中,Fe易失电子作负极、Cu作正极,负极上电极反应式为Fe-2e-=Fe2+,正极上电极反应式为2H++2e-=H2↑,导致负极上金属逐渐减少,正极上有气泡产生,根据得失电子数相等作计算.
解答 解:(1)该原电池中,铁的活泼性大于铜,铁作负极,铁失电子变成离子进入溶液,所以铁片逐渐溶解,电极反应式为:Fe-2e-=Fe2+,
故答案为:负;Fe-2e-=Fe2+;
(2)铜作正极,发生还原反应,铜电极上,氢离子得电子生成氢气2H++2e-=H2↑,所以看到的现象是:有大量气泡产生,
故答案为:有大量气泡产生;还原;
(3)根据负极反应 Fe-2e-=Fe2+,当通过0.6mol电子,Fe的质量理论上减少0.3mol,质量减小16.8g,
故答案为:16.8.
点评 本题考查了原电池电极上的反应现象及电极反应式的书写,写电极反应式时要注意电解质溶液的成分,根据两电极得失电子数相等作计算.

练习册系列答案
相关题目
9.下列说法错误的是( )
| A. | 在共价化合物中不可能含有离子键 | |
| B. | 阴阳离子之间通过静电作用力形成的化学键,叫离子键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 离子化合物中不一定含有金属元素 |
14.燃料电池是一种新型电池,它主要是利用燃料燃烧原理把化学能直接转化为电能,当以30%KOH溶液为电解质溶液,电极反应如下:2H2+4OH--4e-=4H2O,O2+2H2O+4e-=4OH-.据此作出判断,下列说法中不正确的是( )
| A. | 反应时负极附近pH增大 | B. | 电池总反应为2H2+O2=2H2O | ||
| C. | O2在正极发生还原反应 | D. | 工作时OH-向负极移动 |
4.下列说法中,不正确的是( )
| A. | 光合作用是将光能转化为化学能的有效途径 | |
| B. | 煤,石油,天然气都是可再生的化石燃料 | |
| C. | 用植物秸秆制沼气是有效利用生物质能的方式之一 | |
| D. | 开发氢能,太阳能,风能,生物质能等是实现“低碳生活”的有效途径 |
11.沼气的主要成份是CH4,0.5molCH4完全燃烧生成二氧化碳和液态水时放出445kJ热量.下列热化学方程式正确的是( )
| A. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890 kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890kJ/mol | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-445kJ/mol | |
| D. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/mol |
8.下列化学用语正确的是( )
①OH-的电子式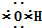
②乙烯的结构简式:CH2=CH2
③甲烷的结构式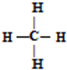
④乙烯的结构式:C2H4.
①OH-的电子式
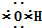
②乙烯的结构简式:CH2=CH2
③甲烷的结构式
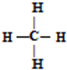
④乙烯的结构式:C2H4.
| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①② |
9.下列有机物溶液在适量的浓度时,不能用于杀菌消毒的是( )
| A. | 苯酚溶液 | B. | 乙醇溶液 | C. | 福尔马林 | D. | 乙酸乙酯溶液 |
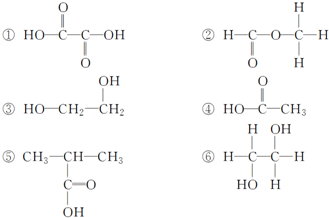
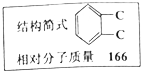 实验室有一试剂瓶的标签严重破损,只能隐约看到如图所示部分,取该试剂瓶中的试剂,通过燃烧实验测得:0.1mol该物质完全燃烧只得到39.6gCO2和9gH2O.
实验室有一试剂瓶的标签严重破损,只能隐约看到如图所示部分,取该试剂瓶中的试剂,通过燃烧实验测得:0.1mol该物质完全燃烧只得到39.6gCO2和9gH2O.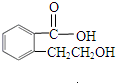 ;
; .
.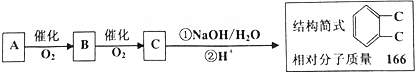
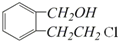 ;
;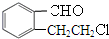 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2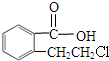 ;
; .
.