题目内容
以下关于元素周期表结构的叙述正确的是( )
| A、元素周期表有7个主族,8个副族 |
| B、元素周期表有3个长周期、4个短周期 |
| C、第ⅢA族位于元素周期表的第三列(从左往右) |
| D、0族位于元素周期表的第18列(从左往右) |
考点:元素周期表的结构及其应用
专题:
分析:A、元素周期表有7个主族、7个副族、1个零族、1个第Ⅷ族;
B、元素周期表有3个短周期、3个短周期,一个不完全;
C、第13列为ⅢA族;
D、第18列为零族元素.
B、元素周期表有3个短周期、3个短周期,一个不完全;
C、第13列为ⅢA族;
D、第18列为零族元素.
解答:
解:A、元素周期表有7个副族,故A错误;
B、元素周期表有3个短周期、3个短周期,一个不完全,故B错误;
C、第3列为ⅢB族,第13列为ⅢA族,故C错误;
D、第18列为零族元素,故D正确;
故选:D.
B、元素周期表有3个短周期、3个短周期,一个不完全,故B错误;
C、第3列为ⅢB族,第13列为ⅢA族,故C错误;
D、第18列为零族元素,故D正确;
故选:D.
点评:本题考查元素周期表的结构,比较基础,注意掌握族与列的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
甲、乙两溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是( )
| A、CO32-、OH-、Cl- |
| B、Cu2+、H+、Cl- |
| C、K+、H+、Cl- |
| D、K+、OH-、CO32- |
设NA为何伏加德罗常数的值,下列叙述正确的是( )
| A、1mol甲醇中含有C-H键数目为4NA |
| B、室温下,PH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C、标准状况下,2.24L已烷含有的分子数目为0.1NA |
| D、常温常压下,46gNO2和N2O4的混合气体中含有的原子数为3NA |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、0.1mol Fe 与0.1mol Cl2充分反应,转移的电子数为0.3 NA |
| B、常温常压下,1mol的氦气和氢气混合气,含有的核外电子数为2NA |
| C、25℃时,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2 NA |
| D、标准状况下,2.24L CCl4和CH2O的混合物中含有NA个碳原子 |
下列氧化还原反应不是发生在同一元素间的是( )
| A、Cl2+H2O═HCl+HClO |
| B、KClO3+6HCl═KCl+3Cl2↑+3H2O |
| C、2FeCl3+H2S═2FeCl2+S↓+2HCl |
| D、2H2O2═2H2O+O2↑ |
下列化学用语表达正确的是( )
| A、溴化钙的化学式是CaBr |
B、HCl分子的电子式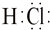 |
| C、乙烯的结构简式:CH2CH2 |
D、氯原子的结构示意图: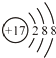 |
下列条件下,离子方程式正确的是( )
| A、电解氯化镁溶液:Mg2++2Cl-═Mg+Cl2↑ |
| B、碳酸镁悬浊液中加醋酸:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O |
| C、酸性K2Cr2O7溶液可氧化双氧水H2O2:Cr2O72-+8H++5H2O2=2 Cr3++4O2↑+9H2O |
| D、氨水溶解氯化银沉淀的原理:AgCl+2 NH3?H2O=[Ag(NH3)2]++Cl-+2H2O |
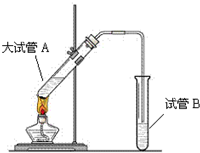 “酒是陈年的香”,是因为乙醇被少量氧气氧化,氧化产物与乙醇反应生成有香味的物质,实验室可以模拟后一过程.
“酒是陈年的香”,是因为乙醇被少量氧气氧化,氧化产物与乙醇反应生成有香味的物质,实验室可以模拟后一过程.