题目内容
甲、乙两溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是( )
| A、CO32-、OH-、Cl- |
| B、Cu2+、H+、Cl- |
| C、K+、H+、Cl- |
| D、K+、OH-、CO32- |
考点:离子共存问题
专题:离子反应专题
分析:甲溶液呈蓝色,应含有Cu2+,则与Cu2+反应的离子应存在于乙中,结合溶液的电中性原则解答.
解答:
解:甲溶液呈蓝色,应含有Cu2+,因CO32-、OH-可与反应生成沉淀,则只能存在于乙中,乙中含有CO32-、OH-,则一定不存在H+,阳离子只能为K+,则乙中含有CO32-、OH-、K+,甲中含有Cu2+、H+、Cl-,
故选D.
故选D.
点评:本题考查离子共存问题,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合运用的考查,注意把握离子之间发生复分解反应的特点,难度中等.

练习册系列答案
相关题目
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A、生成40.0LN2(标准状况) |
| B、有0.250molKNO3被氧化 |
| C、转移电子的物质的量为2.5mol |
| D、被氧化的N原子的物质的量为3.75mol |
已知金属钾有如下性质:①钾的密度比水小;②钾的熔点低;③钾与水反应时放出热量;④钾与水反应后溶液呈碱性.某学生将一小块金属钾投入滴有酚酞溶液的水中,以上实验能证明上述四点性质中的( )
| A、①④ | B、①②④ |
| C、①③④ | D、①②③④ |
对于可逆反应N2(g)+3H2(g)
2NH3(g),在不同条件下的化学全品高考网“反应速率如下,其中表示反应速率最快的是( )
| 催化剂 |
| 高温高压 |
| A、υ(H2)=0.3mol/(L?min) |
| B、υ(N2)=0.2mol/(L?min) |
| C、υ(NH3)=0.25mol/(L?min) |
| D、υ(H2)=0.4mol/(L?min) |
下列装置能形成原电池的是( )
A、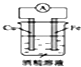 |
B、 |
C、 |
D、 |
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A、W得电子能力比Q强 |
| B、由Z与Y组成的物质在熔融时能导电 |
| C、钠与Y可能形成Na2Y2化合物 |
| D、X有多种同素异形体,而Y不存在同素异形体 |
以下关于元素周期表结构的叙述正确的是( )
| A、元素周期表有7个主族,8个副族 |
| B、元素周期表有3个长周期、4个短周期 |
| C、第ⅢA族位于元素周期表的第三列(从左往右) |
| D、0族位于元素周期表的第18列(从左往右) |
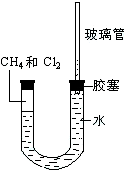 如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.