题目内容
下列氧化还原反应不是发生在同一元素间的是( )
| A、Cl2+H2O═HCl+HClO |
| B、KClO3+6HCl═KCl+3Cl2↑+3H2O |
| C、2FeCl3+H2S═2FeCl2+S↓+2HCl |
| D、2H2O2═2H2O+O2↑ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:有元素化合价变化的反应为氧化还原反应,化合价升高的元素被氧化,化合价降低的元素被还原,分析反应中元素化合价变化即可.
解答:
解:A、只有Cl元素的价态变化,故A错误;
B、只有Cl元素的价态变化,故B错误;
C、Fe元素和S元素的价态发生变化,故C正确;
D、只有O元素的价态发生变化,故D错误.
故选C.
B、只有Cl元素的价态变化,故B错误;
C、Fe元素和S元素的价态发生变化,故C正确;
D、只有O元素的价态发生变化,故D错误.
故选C.
点评:本题考查了氧化还原反应的概念,注意从化合价变化分析,题目难度不大.

练习册系列答案
相关题目
已知金属钾有如下性质:①钾的密度比水小;②钾的熔点低;③钾与水反应时放出热量;④钾与水反应后溶液呈碱性.某学生将一小块金属钾投入滴有酚酞溶液的水中,以上实验能证明上述四点性质中的( )
| A、①④ | B、①②④ |
| C、①③④ | D、①②③④ |
设NA为阿伏加德罗常数的值.下列说法正确是( )
| A、标准状况下,2.24 L三氯甲烷中含有碳氯共价健的数目为0.3NA |
| B、25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
| C、常温常压下,28 g C2H4、C3H6的混合气体中含有碳原子的数目为2NA |
| D、0.1 mol Cl2全部溶于水后转移电子的数目为0.1NA |
设NA为阿伏加德罗常数的值,则下列说法正确的是( )
| A、电解精炼铜时,若阴极得到电子数为2NA,阳极减少64g |
| B、200mL某硫酸强碱盐中含有1.5NA个SO42-离子,同时含有NA个金属阳离子,该盐物质的量浓度是2.5mol/L |
| C、常温常压下78g Na2O2固体中所含阴、阳离子总数为4NA |
| D、一定条件下足量的Fe粉与浓硫酸反应,转移电子数一定为2NA |
下列离子方程式书写正确的是( )
| A、AlCl3溶液滴加过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++H2O |
| B、硫酸和氢氧化钡溶液反应:H++SO42-+OH-+Ba2+=BaSO4↓+H2O |
| C、向氢氧化铁胶体中滴加足量HI溶液:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| D、向氯化钙溶液中通入CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
以下关于元素周期表结构的叙述正确的是( )
| A、元素周期表有7个主族,8个副族 |
| B、元素周期表有3个长周期、4个短周期 |
| C、第ⅢA族位于元素周期表的第三列(从左往右) |
| D、0族位于元素周期表的第18列(从左往右) |
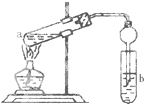 如图,在试管a中先加入3mL 95%的乙醇,边摇动边缓缓加入2mL浓H2SO4并充分摇匀,冷却后再加入2mL冰醋酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
如图,在试管a中先加入3mL 95%的乙醇,边摇动边缓缓加入2mL浓H2SO4并充分摇匀,冷却后再加入2mL冰醋酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.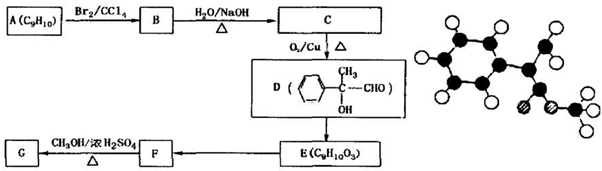
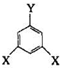 表示(其中X、Y均不为H),且能发生银镜反应的物质有
表示(其中X、Y均不为H),且能发生银镜反应的物质有