题目内容
7.软锰矿(主要成分为MnO2)可用于制备锰及其化合物.(1)早期冶炼金属锰的一种方法是先煅烧软锰矿生成Mn3O4,再利用铝热反应原理制得锰,该铝热反应的化学方程式为8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn.
(2)现代冶炼金属锰的一种工艺流程如下图所示:
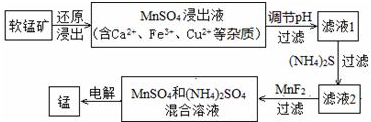
下表为t℃时,有关物质的pKsp(注:pKsp=-lgKsp).
| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
12MnO2+C6H12O6+12H2SO4=12MnSO4+CO2↑+18H2O
①该反应中,还原剂为C6H12O6.写出一种能提高还原浸出速率的措施:升高反应温度或将软锰矿研细等.
②滤液1的pH>(填“>”、“<”或“=”)MnSO4浸出液的pH.
③加入MnF2的主要目的是除去Ca2+(填Ca2+、Fe3+或Cu2+)
(3)由MnSO4制取MnCO3
往MnSO4溶液中加入过量NH4HCO3溶液,该反应的离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;若往MnSO4溶液中加入(NH4)2CO3溶液,还会产生Mn(OH)2,可能的原因有:MnCO3(s)+2OH-(aq)?Mn(OH)2(s)+CO32-(aq),t℃时,计算该反应的平衡常数K=100(填数值).
分析 (1)高温条件下,Al和Mn3O4发生置换反应生成Mn和氧化铝;
(2)软锰矿还原浸出得到MnSO4溶液,说明浸取液为稀硫酸,同时溶液中还含有Ca2+、Fe3+、Cu2+等杂质,调节溶液的pH,Fe(OH)3pKap为37.4与其它离子相比最大,调节pH可以将 Fe(OH)3沉淀下来,向滤液中加入硫化铵,CuSpKap为35.2,可以将铜离子形成硫化物沉淀下来,再加入MnF2,形成CaF2沉淀,除去Ca2+,最后对得到的含有锰离子的盐电解,可以得到金属Mn;
①该反应中Mn元素化合价由+4价变为+2价、C元素化合价由0价变为+4价,失电子化合价升高的反应物是还原剂;增大反应物浓度、升高温度、增大反应物接触面积都能增大反应速率;
②软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4=12MnSO4+6CO2↑+18H2O,溶液呈强酸性,还原浸出液中含有Mn2+、Ca2+、Fe3+、Cu2+,此时未形成沉淀,Kp为电离平衡常数,pKp=-1gKp,pKp越大,沉淀溶解平衡常数越小,滤液1为形成Fe(OH)3沉淀,pKp=-1gKp=37.4,Kp=10-37.4,Kp=c(Fe3+)×c3(OH-)=10-37.4,c(OH-)≈10-10,c(H+)=1×10-4mol/L,pH=4,据此判断pH大小;
③加入MnF2的目的除去形成CaF2沉淀,除去Ca2+;
(3)锰离子和碳酸氢根离子发生双水解反应生成碳酸锰沉淀;由MnCO3(s)+2OH-(aq)?Mn(OH)2(s)+CO32-(aq)可知,K=$\frac{c(C{{O}_{3}}^{2-})}{{c}^{2}(O{H}^{-})}$=$\frac{\frac{{K}_{sp}(MnC{O}_{3})}{c(M{n}^{2+})}}{\frac{{K}_{sp}[Mn(OH)_{2}]}{c(M{n}^{2+})}}$.
解答 解:(1)高温条件下,Al和Mn3O4发生置换反应生成Mn和氧化铝,反应方程式为8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn,故答案为:8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn;
(2)软锰矿还原浸出得到硫酸锰溶液,说明浸取液为稀硫酸,同时溶液中还含有Ca2+、Fe3+、Cu2+等杂质,调节溶液的pH,Fe(OH)3pKap为37.4与其它离子相比最大,调节pH可以将 Fe(OH)3沉淀下来,向滤液中加入硫化铵,CuSpKap为35.2,可以将铜离子形成硫化物沉淀下来,再加入MnF2,形成CaF2沉淀,除去Ca2+,最后对得到的含有锰离子的盐电解,可以得到金属锰,
①软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4═12MnSO4+6CO2↑+18H2O,该反应中,Mn元素化合价由+4价变为+2价、C元素化合价由0价变为+4价,失电子化合价升高的反应物是还原剂,所以C6H12O6为还原剂;
反应物接触面积越大、温度越高反应速率越快,所以能提高还原浸出速率的措施:升高反应温度或将软锰矿研细等,
故答案为:C6H12O6;升高反应温度或将软锰矿研细等;
②软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4=12MnSO4+6CO2↑+18H2O,溶液呈强酸性,还原浸出液中含有Mn2+、Ca2+、Fe3+、Cu2+,此时未形成沉淀,Kp为电离平衡常数,pKp=-1gKp,pKp越大,沉淀溶解平衡常数越小,滤液1为形成Fe(OH)3沉淀,pKp=-1gKp=37.4,Kp=10-37.4,Kp=c(Fe3+)×c3(OH-)=10-37.4,c(OH-)≈10-10,c(H+)=1×10-4mol/L,pH=4,所以滤液1的pH大于MnSO4浸出液的pH=4才能形成氢氧化铁沉淀,
故答案为:>;
③CaF2难溶于水,滤液2为Mn2+、Ca2+、NH4+、SO42-,加入MnF2的目的除去形成CaF2沉淀,除去Ca2+,故答案为:Ca2+;
(3)锰离子和碳酸氢根离子反应生成碳酸锰沉淀、水和二氧化碳气体,离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;由MnCO3(s)+2OH-(aq)?Mn(OH)2(s)+CO32-(aq)可知K=$\frac{c(C{{O}_{3}}^{2-})}{{c}^{2}(O{H}^{-})}$=$\frac{\frac{{K}_{sp}(MnC{O}_{3})}{c(M{n}^{2+})}}{\frac{{K}_{sp}[Mn(OH)_{2}]}{c(M{n}^{2+})}}$=$\frac{1{0}^{-10.7}}{1{0}^{-12.7}}$=100,
故答案为:Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;100.
点评 本题考查物质分离和提纯和制备,为高频考点,涉及难溶物的溶解平衡、离子方程式书写、氧化还原反应等知识点,侧重考查基本理论,难点是难溶物溶解平衡计算,题目难度中等,熟悉流程图中发生的反应及基本操作方法.

 53随堂测系列答案
53随堂测系列答案| A. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| B. | 乙醇溶液、臭氧、双氧水、高锰酸钾溶液均可用于消毒杀菌,且原理不同 | |
| C. | 生石灰、铁粉、硅胶是食品包装中常用的干燥剂 | |
| D. | 纯碱是焙制糕点所用的发酵粉的主要成分之一,也可用纯碱除去物品表面的油污 |
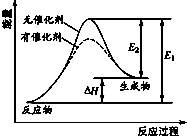
| A. | 该反应为放热反应 | |
| B. | 催化剂能降低该反应的焓变 | |
| C. | 催化剂能降低E2的值 | |
| D. | 逆反应的活化能大于正反应的活化能 |
| A. | 125 mL | B. | 275 mL | C. | 325 mL | D. | 450 mL |
| A. | 萃取溴水中的溴,将四氯化碳和溴水混合后,振荡并打开分液漏斗瓶塞,使漏斗内气体放出 | |
| B. | 在蔗糖中加入浓硫酸时,蔗糖变黑,证明浓硫酸具有脱水性 | |
| C. | 向Ba(NO3)2溶液中通入SO2气体,产生白色沉淀,可推测SO2与可溶性钡盐均能反应产生白色沉淀 | |
| D. | 若要检验铜和浓硫酸反应后产物硫酸铜,可向反应后的试管中加入少量水,观察溶液是否变蓝,若变蓝则证明有硫酸铜生成 |
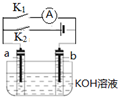
| A. | 断开K2,闭合K1一段时间,溶液的pH要变大 | |
| B. | 断开K1,闭合K2时,b极上的电极反应式为 2H++2e-═H2↑ | |
| C. | 断开K1,闭合K2时,OH-向b极移动 | |
| D. | 断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-═O2↑+2H2O |
| A. | 22 | B. | 24 | C. | 20 | D. | 25 |
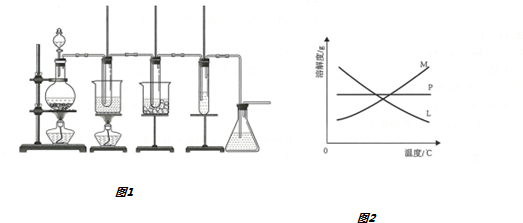
Ⅰ.在实验室用图1装置制取氯酸钾、次氯酸钠并探究氯水的性质
图1中:①为氯气发生装置;
②中试管里盛有15mL30%KOH溶液,并置于水浴中;
③中试管里盛有15mL8%NaOH溶液,并置于冰水浴中;
④中试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
回答下列问题
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B(填写编号字母)的净化装置.
A.碱石灰 B.饱和食盐水
C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是碱溶液(或反应物)的浓度不同,反应温度不同反应完毕经冷却后,②的试管中有大量晶体析出,图2中符合该晶体溶解度变化规律的曲线是M(填写编号字母);从②的试管中分离出该晶体的方法是过滤(填写实验操作名称)
(3)本实验中制取次氯酸钠的离子方程式是Cl2+2OH-═ClO-+Cl-+H2O
(4)实验中可观察到④的试管里溶液颜色发生了如下变化,请填写表中空白:
| 实验现象 | 原因 |
| 溶液从初的紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊试液变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为黄绿色 | 继续通入的氯气溶于水使溶液呈黄绿色 |
(5)将硫酸溶液滴入图3烧杯中,至溶液显酸性,结果也有Cl2生成,该反应的离子方程式是Cl-+ClO-+2H+=Cl2+H2O;
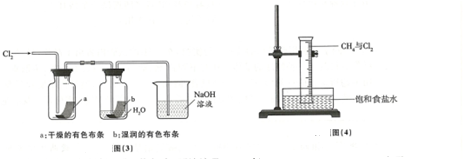
(6)将图4装置放置在光亮的地方(日光不直接照射),一段时间后,观察到量筒内壁上有油状液滴生成,量筒内液面上升.油状液地的成分可能是CH2Cl2、CHCl3、CCl4 (写分子式);量筒内液面上升的原因是氯化氢极易溶于水,量筒中压强减小,液面上升.
| A. | Ca(OH)═Ca2++2OH- | B. | KNO3═K++NO3- | C. | NH4Cl═4NH++Cl- | D. | H2SO4═2H++SO42- |