题目内容
9.科研、生产和生活中的下列做法利用了氧化还原反应的是( )| A. | 用乙醚从黄花蒿中提取青蒿素 | B. | 由青蒿素( )合成双氢青蒿素( )合成双氢青蒿素( )的反应 )的反应 | ||
| C. | 空气净化器过滤净化空气 | D. | 消毒柜通电产生臭氧的过程 |
分析 含元素化合价变化的反应为氧化还原反应,有机反应中加O去H为氧化反应,加H去O为还原反应,结合发生的反应及元素的化合价判断.
解答 解:A.用乙醚从黄花蒿中提取青蒿素为萃取原理,为物理变化,故A不选;
B.由青蒿素( )合成双氢青蒿素(
)合成双氢青蒿素( )的反应,C=O转化为-OH,分子中加H,为还原反应,故B选;
)的反应,C=O转化为-OH,分子中加H,为还原反应,故B选;
C.空气净化器过滤净化空气,为过滤原理,为物理变化,故C不选;
D.消毒柜通电产生臭氧的过程,氧气转化为臭氧,没有元素的化合价变化,为非氧化还原反应,故D不选;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意有机物氧化还原反应的判断,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
19.N2+3H2?2NH3反应达到平衡时的说法不正确的是( )
| A. | 平衡体系中氮气、氢气、氨的物质的量保持不变 | |
| B. | 平衡体系中氮气、氢气、氨的浓度保持不变 | |
| C. | 单位时间内生成的氨和分解的氨物质的量相同 | |
| D. | 单位时间内消耗的氮气和氢气与生成的氨气物质的量相同 |
17.下面的排序不正确的是( )
| A. | 沸点由高到低:HF>HCl | B. | 熔点由高到低:K>Li | ||
| C. | 硬度由大到小:金刚石>晶体硅 | D. | 晶格能由大到小:NaF>NaCl |
4.下列物质中,含有非极性键的离子化合物是( )
| A. | CaCl2 | B. | Ba(OH)2 | C. | H2O2 | D. | Na2O2 |
1.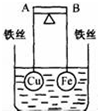 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )| A. | 杠杆为导体和绝缘体时,均为A 端高B 端低 | |
| B. | 杠杆为导体和绝缘体时,均为A 端低B 端高 | |
| C. | 当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低 | |
| D. | 当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高 |
18.硼酸(H3BO3)微溶于水,其水溶液显弱酸性,对人体的受伤组织有防腐作用.工业上以硼镁矿(Mg2B2O5•H2O)为原料生产硼酸,同时以硼镁泥为原料制取硫酸镁,可用于印染、造纸、医药等工业.生产工艺流程如下图所示,请回答下列问题:
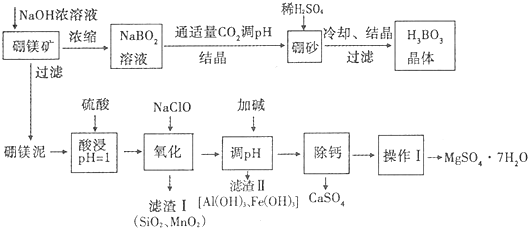
注:
①硼镁泥的主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质.
②硼酸电离平衡常数K=5.8×10-10
③
④已知MgSO4、CaSO4的溶解度如下表:
(1)写出上述流程中生成硼砂(Na2B4O7)的离子方程式4BO2-+CO2=B4O72-+CO32-
(2)硼酸根离子可表示为B(OH)4-.写出硼酸电离的方程式H3BO3+H2O?B(OH)4-+H+
(3)N滴定法测定硼酸晶体的纯度.研究结果表明,用0.1mol•L-1NaOH溶液直接滴定硼酸溶液,滴定过程如曲线①所示,向硼酸溶液中加入多元醇后再滴定如曲线②所示.请分析,能否用强碱直接滴定硼酸溶液,不能 (填“能”或“不能”),理由是:没有明显的pH突变区域,无法判断终点,会造成较大的误差
(4)向硼镁泥酸浸后的溶液中,加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是ClO-+Mn2++H2O=MnO2↓+Cl-+2H+.
(5)加碱调节至pH为4.7时,杂质离子便可完全沉淀.(离子浓度小于或等于1×l0-5mol•L-1时,即可认为该离子沉淀完全)
(6)“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤蒸发浓缩结晶、趁热过滤.
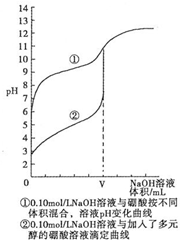

注:
①硼镁泥的主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质.
②硼酸电离平衡常数K=5.8×10-10
③
| 化合物 | Mg(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| Ksp近似值 | 10-11 | 10-16 | 10-38 | 10-33 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(2)硼酸根离子可表示为B(OH)4-.写出硼酸电离的方程式H3BO3+H2O?B(OH)4-+H+
(3)N滴定法测定硼酸晶体的纯度.研究结果表明,用0.1mol•L-1NaOH溶液直接滴定硼酸溶液,滴定过程如曲线①所示,向硼酸溶液中加入多元醇后再滴定如曲线②所示.请分析,能否用强碱直接滴定硼酸溶液,不能 (填“能”或“不能”),理由是:没有明显的pH突变区域,无法判断终点,会造成较大的误差
(4)向硼镁泥酸浸后的溶液中,加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是ClO-+Mn2++H2O=MnO2↓+Cl-+2H+.
(5)加碱调节至pH为4.7时,杂质离子便可完全沉淀.(离子浓度小于或等于1×l0-5mol•L-1时,即可认为该离子沉淀完全)
(6)“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤蒸发浓缩结晶、趁热过滤.

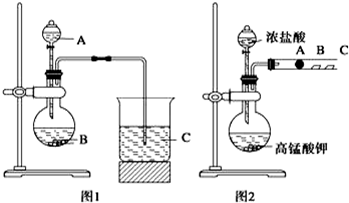
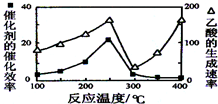 CH4和CO2可以制造价值更高的化学产品.已知:
CH4和CO2可以制造价值更高的化学产品.已知: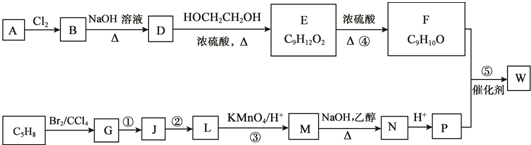
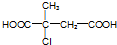 .
. ;D中含氧官能团的名称是羟基;④的反应类型是消去反应.
;D中含氧官能团的名称是羟基;④的反应类型是消去反应.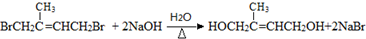 .
. .
. .
.