题目内容
17.下面的排序不正确的是( )| A. | 沸点由高到低:HF>HCl | B. | 熔点由高到低:K>Li | ||
| C. | 硬度由大到小:金刚石>晶体硅 | D. | 晶格能由大到小:NaF>NaCl |
分析 A.HF分子之间含氢键;
B.碱金属单质的熔点从上到下减小;
C.原子晶体中,半径小的硬度大;
D.离子晶体中,离子键小的晶格能大.
解答 解:A.HF分子之间含氢键,则沸点由高到低:HF>HCl,故A正确;
B.碱金属单质的熔点从上到下减小,则熔点由高到低:Li>K,故B错误;
C.原子晶体中,半径小的硬度大,半径为C<Si,则硬度由大到小:金刚石>晶体硅,故C正确;
D.离子晶体中,离子键小的晶格能大,离子半径F-<Cl-,则晶格能由大到小:NaF>NaCl,故D正确;
故选B.
点评 本题考查周期表和周期律及物质结构,为高频考点,把握性质的比较方法、物质结构与性质等为解答该题的关键,侧重分析与应用能力的考查,注意晶体类型及性质比较,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
7.联苯(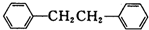 )是一种重要的有机合成中间体,实验室可用苯和1,2-二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2-二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
(一)催化剂的制备
如图是实验室制取少量无水AlCl3的相关实验装置的仪器和药品
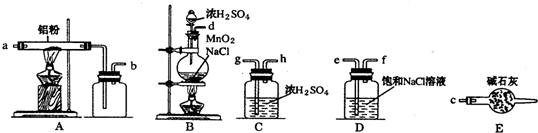
(1)将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d接e,f接g,h接a,b接c.
(2)有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl3,你认为是否可行不可行 (填“可行”或“不可行”),你的理由是制得的Cl2中混有的HCl与Al反应生成H2,H2与Cl2混合加热时会发生爆炸.
(3)装置A中隐藏着一种安令隐患,请提出一种改进方案:在硬质玻璃管与广口瓶之间用粗导管连接,防止AlCl3冷凝成固体造成堵塞.
(二)联苯的制备
联苯的制取原理为: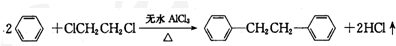
反应最佳条件为n(苯):n(1,2-二氯乙烷)=10:1,反应温度在60-65℃之间.实验室制取联苯的装置如图所示(加热和加持仪器略去)

实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7 mL 1,2-二氯乙烷,控制反应速度在60-65℃,反应约60 min.将反应后的化合物依次用稀盐酸、2% Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,在减压蒸馏收集170〜172℃的馏分,得联苯18.2 g.
相关物理常数和物理性质如表
(4)仪器a的名称为球形冷凝管,和普通分液漏斗相比,使用滴液漏斗的优点是可以使液体顺利滴下.
(5)洗涤操作中,水洗的目的是洗掉Na2CO3(或洗掉可溶性无机物),无水硫酸镁的作用是吸水剂(干燥剂).
(6)常压蒸馏时,最低控制温度是83.5℃.
(7)该实验的产率约为72.85% (小数点后保留两位有效数字).
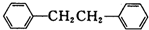 )是一种重要的有机合成中间体,实验室可用苯和1,2-二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2-二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:(一)催化剂的制备
如图是实验室制取少量无水AlCl3的相关实验装置的仪器和药品

(1)将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d接e,f接g,h接a,b接c.
(2)有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl3,你认为是否可行不可行 (填“可行”或“不可行”),你的理由是制得的Cl2中混有的HCl与Al反应生成H2,H2与Cl2混合加热时会发生爆炸.
(3)装置A中隐藏着一种安令隐患,请提出一种改进方案:在硬质玻璃管与广口瓶之间用粗导管连接,防止AlCl3冷凝成固体造成堵塞.
(二)联苯的制备
联苯的制取原理为:

反应最佳条件为n(苯):n(1,2-二氯乙烷)=10:1,反应温度在60-65℃之间.实验室制取联苯的装置如图所示(加热和加持仪器略去)

实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7 mL 1,2-二氯乙烷,控制反应速度在60-65℃,反应约60 min.将反应后的化合物依次用稀盐酸、2% Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,在减压蒸馏收集170〜172℃的馏分,得联苯18.2 g.
相关物理常数和物理性质如表
| 名称 | 相对分子质量 | 密度/(g•cm-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
| 1,2-二氯乙烷 | 99 | 1.27 | -35.3 | 83.5 | 难溶水,可溶苯 |
| 无水氯化铝 | 133.5 | 2.44 | 190 | 178(升华) | 遇水水解,微溶苯 |
| 联苄 | 182 | 0.98 | 52 | 284 | 难溶水,易溶苯 |
(5)洗涤操作中,水洗的目的是洗掉Na2CO3(或洗掉可溶性无机物),无水硫酸镁的作用是吸水剂(干燥剂).
(6)常压蒸馏时,最低控制温度是83.5℃.
(7)该实验的产率约为72.85% (小数点后保留两位有效数字).
8.人体内的营养物质中含量最多且又不是属于有机物的是( )
| A. | 无机盐 | B. | 油脂 | C. | 水 | D. | 蛋白质 |
5.下列说法不正确的是( )
| A. | 一般情况下,σ键比π键重叠程度大,形成的共价键更强 | |
| B. | 两个原子之间形成共价键时,最多有一个σ键 | |
| C. | 气体单质分子中,一定有σ键,可能有π键 | |
| D. | 杂化轨道只用于形成σ键或者用来容纳未参与成键的孤电子对 |
12.巴豆酸的结构简式为CH3-CH═CH-COOH.现有下列物质,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是( )
①氯化氢 ②溴水 ③纯碱溶液 ④2-丁醇 ⑤酸性KMnO4溶液.
①氯化氢 ②溴水 ③纯碱溶液 ④2-丁醇 ⑤酸性KMnO4溶液.
| A. | ②④⑤ | B. | ①③④ | C. | ①②③④ | D. | ①②③④⑤ |
9.科研、生产和生活中的下列做法利用了氧化还原反应的是( )
| A. | 用乙醚从黄花蒿中提取青蒿素 | B. | 由青蒿素( )合成双氢青蒿素( )合成双氢青蒿素( )的反应 )的反应 | ||
| C. | 空气净化器过滤净化空气 | D. | 消毒柜通电产生臭氧的过程 |
6.已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是( )
| A. | X、Y、Z、W的原子半径依次减小 | |
| B. | W与X形成的化合物中只含离子键 | |
| C. | 非金属性:Z>W | |
| D. | 若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
7.有关0.1mol/LNa2SO3溶液的说法正确的是( )
| A. | 由于水解,溶液中n(SO32-)<0.1mol | |
| B. | 加入少量NaOH固体,c(SO32-)与c(Na+)均增大 | |
| C. | c(Na+)+c(H+)=2c(SO32-)+2c(HSO3-)+c(OH-) | |
| D. | 2c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |
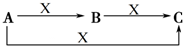 A、B、C、X是中学化学常见的物质,它们之间的转化关系如图所示(反应条件和部分产物省略).请回答下列问题:
A、B、C、X是中学化学常见的物质,它们之间的转化关系如图所示(反应条件和部分产物省略).请回答下列问题: