题目内容
8.金属元素Al、Co、Cu可与C、H、N、O、S等形成多种化合物.(1)C、N、O、S四种元素的第一电离能由小到大的顺序为C<S<O<N.
(2)Co、Cu原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①将无水硫酸铜溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.此配合离子空间构型为平面正方形,请写出生成此配合离子的离子方程式:Cu2++4H2O=[Cu(H2O)4]2+
②Co (NH3)5BrSO4可形成两种配合物,已知Co3+的配位数是6,为了确定配合物Co (NH3)5BrSO4的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为[Co(SO4)(NH3)5]Br,
(3)根据元素原子的外围电子排布特征,将周期表分成五个区域,其中Co属于d区.
(4)Al单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
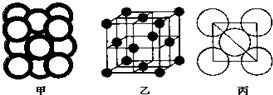
Al单质晶体中原子的配位数为12.若已知Al的原子半径为r,NA代表阿伏加德罗常数,Al的相对原子质量为M;该晶体的密度为$\frac{M}{4\sqrt{2}{N}_{A}{r}^{3}}$(用字母表示).
分析 (1)同一主族中,从上向下,元素第一电离能逐渐减小,同一周期中,元素的第一电离能随着原子序数的增大而增大,但N元素的最外层电子处于半满状态,是一种稳定结构,所以它的第一电离能高于同周期相邻的元素,据此判断;
(2)①硫酸铜溶于水,铜离子与水生成了呈蓝色的配合离子[Cu(H2O)4]2+,该络合离子为平面正方形;
②Co(NH3)5BrSO4可形成两种配合物,Co3+的配位数是6,在第一种配合物的溶液中加BaCl2 溶液时,产生白色沉淀,该物质可以电离出SO42-,故配体为NH3、Br-,该物质结构为[Co(NH3)5Br]SO4,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,该物质不能电离出SO42-,故配体为NH3、SO42-,该物质为[Co(NH3)5SO4]Br;
(3)d区包含ⅢB~ⅦB(镧系元素、锕系元素除外)、第Ⅷ族,据此判断;
(4)由晶胞结构可知,以顶点Al原子为研究对象,与之最近的Al原子处于面心上,结合Al的摩尔质量计算晶胞质量,Al的原子半径为r,则晶胞棱长为$2\sqrt{2}$r,再根据ρ=$\frac{m}{V}$计算晶胞密度.
解答 解:(1)同一主族中,从上向下,元素第一电离能逐渐减小,同一周期中,元素的第一电离能随着原子序数的增大而增大,但N元素的最外层电子处于半满状态,是一种稳定结构,所以它的第一电离能高于同周期相邻的元素,所以C、N、O、S四种元素的第一电离能由小到大的顺序为C<S<O<N,
故答案为:C<S<O<N;
(2)①硫酸铜溶于水,铜离子与水生成了呈蓝色的配合离子[Cu(H2O)4]2+,离子方程式为Cu2++4H2O=[Cu(H2O)4]2+,该络合离子为平面正方形,
故答案为:平面正方形;Cu2++4H2O=[Cu(H2O)4]2+;
②Co(NH3)5BrSO4可形成两种配合物,Co3+的配位数是6,在第一种配合物的溶液中加BaCl2 溶液时,产生白色沉淀,该物质可以电离出SO42-,故配体为NH3、Br-,该物质结构为[Co(NH3)5Br]SO4,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,该物质不能电离出SO42-,故配体为NH3、SO42-,该物质为[Co(NH3)5SO4]Br,
故答案为:[Co(NH3)5SO4]Br;
(3)Co属于第Ⅷ族元素,所以Co属于d区,
故答案为:d;
(4)由晶胞结构图可知,以顶点原子为研究对象,与之最近的原子处于面心上,每个顶点原子为12个面共用,故晶胞中该原子的配位数为12,晶胞中Al原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞质量为4×$\frac{M}{{N}_{A}}$,Al的原子半径为r,则晶胞棱长为$2\sqrt{2}$r,故Al晶胞的密度ρ=$\frac{m}{V}$=4×$\frac{M}{{N}_{A}}$÷($2\sqrt{2}$r)3=$\frac{M}{4\sqrt{2}{N}_{A}{r}^{3}}$,
答:12;$\frac{M}{4\sqrt{2}{N}_{A}{r}^{3}}$.
点评 本题考查第一电离能的比较、配合物的形成和结构判断、晶胞计算,注意利用均摊法计算晶胞质量,需要学生具有一定的数学计算能力,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 可以用分液漏斗分离硝基苯和苯 | |
| B. | 加浓溴水,然后过滤可以除去苯中少量乙烯 | |
| C. | 苯、溴水、铁粉混合制得溴苯 | |
| D. | 用溴水可以鉴别苯、乙醇、苯乙烯( ) ) |
①用滴管吸取水样,然后用精密pH试纸测其pH
②将水样分成3份
③用同样的方法测定另2份水样
④用滴管吸取水样,然后用广泛pH试纸测其pH
正确的实验顺序为( )
| A. | ②④③① | B. | ②④①③ | C. | ②①④③ | D. | ④②①③ |
| A. | 碳酸钙溶于醋酸CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 锌片插入硝酸银溶液中Zn+Ag+═Zn2++Ag | |
| C. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| D. | 硫酸镁溶液和氢氧化钡溶液反应 SO42-+Ba2+═BaSO4↓ |
部分短周期元素的原子半径及主要化合价列表
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | M与T、Q与 T形成的化合物性质相似 | D. | L2+与R2-的核外电子数相等 |

| I | Ii | Iii | |
| 备选装置 |  |  |  |
a.烧碱 b.生石灰. c.二氧化硅 d.五氧化二磷
(2)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择并将编号填入下列空格.BⅠ;DⅡ;EⅢ(填编号).装置I中需要的试剂是碱石灰.
(3)写出F中发生反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(4)装置C内出现白烟并在容器内壁凝结,鉴定该固体中的阳离子的操作步骤:取固体适量,加入浓氢氧化钠溶液并加热,产生能使湿润的红色石蕊试纸变蓝色的气体,可证明阳离子为氨根离子.
(5)该装置连接后尚存在的缺陷是:缺少尾气处理装置,污染环境.
| A. | Q1>Q2 | B. | Q1<Q2 | C. | Q1=Q2 | D. | 无法确定 |
| A. | 升高温度可使该反应的正逆反应速率同时增大 | |
| B. | 单位时间内消耗CO和NO的物质的量相等时,反应达到平衡 | |
| C. | 反应达到平衡后,NO的反应速率保持恒定 | |
| D. | 使用高效催化剂可增大反应速率 |
 ,反应类型:取代反应.
,反应类型:取代反应.