题目内容
18.汽车尾气无害化处理反应为2NO(g)+2CO(g)═N2(g)+2CO2(g).下列说法错误的是( )| A. | 升高温度可使该反应的正逆反应速率同时增大 | |
| B. | 单位时间内消耗CO和NO的物质的量相等时,反应达到平衡 | |
| C. | 反应达到平衡后,NO的反应速率保持恒定 | |
| D. | 使用高效催化剂可增大反应速率 |
分析 A.升高温度,增大活化分子百分数,导致正逆反应速率都增大;
B.无论是否达到平衡状态,单位时间内消耗CO、NO的物质的量都相等;
C.当反应达到平衡状态时,同一物质的正逆反应速率相等且不变;
D.正催化剂能同等程度的增大正逆反应速率.
解答 解:A.升高温度,增大活化分子百分数,导致正逆反应速率都增大,故A正确;
B.无论是否达到平衡状态,单位时间内消耗CO、NO的物质的量都相等,所以单位时间内消耗CO和NO的物质的量相等时,该反应不一定达到平衡状态,故B错误;
C.当反应达到平衡状态时,同一物质的正逆反应速率相等且不变,所以反应达到平衡后,NO的反应速率保持恒定且不为0,故C正确;
D.催化剂能增大活化分子百分数,所以正催化剂能同等程度的增大正逆反应速率,所以使用高效催化剂可增大反应速率,故D正确;
故选B.
点评 本题考查化学反应速率影响因素,为高频考点,明确温度、催化剂、浓度对化学反应速率影响原理即可解答,注意催化剂只影响反应速率但不影响平衡移动.

练习册系列答案
相关题目
9.把一套以液化石油气(主要成分为C3H8和C4H10)为燃料的炉灶,现改用天然气(主要成分为CH4)为燃料,需要调整进入炉灶的燃料和空气的量.正确方法为( )
| A. | 只需调大燃料气的进气量 | B. | 只需调大空气的进气量 | ||
| C. | 同时调大燃料气和空气的量 | D. | 同时调小燃料气和空气的量 |
3.已知:锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
| A. | 1:4 | B. | 1:9 | C. | 1:8 | D. | 1:2 |
10.下列个反应中,符合如图所示能量变化的是( )
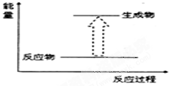

| A. | 乙醇与水反应 | |
| B. | 氧化钙与水反应 | |
| C. | 甲烷在氧气中燃烧 | |
| D. | 氢氧化钡晶体[Ba(OH)2•8H2O]与氯化铵晶体混合反应 |
7.1869年俄国化学家门捷列夫在前人研究元素分类的基础上,提出了元素周期律,并列出了第一张元素周期表,门捷列夫是按照什么递增来制定周期表的( )
| A. | 相对原子质量的递增 | B. | 原子序数的递增 | ||
| C. | 元素化合价的递增 | D. | 原子半径递增 |
8.实验室保存下列物质的方法中,不正确的是( )
| A. | 少量金属钠保存在煤油里 | |
| B. | 烧碱溶液盛装在使用玻璃塞的试剂瓶中 | |
| C. | 新制氯水通常保存在棕色试剂瓶中 | |
| D. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 |

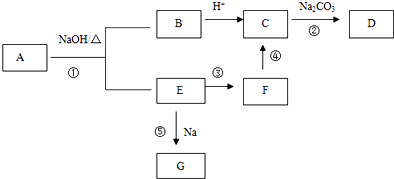
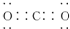 ;
;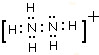 ;
;