题目内容
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L的戊烷所含的分子数为0.5 NA |
| B、26g乙炔所含共用电子对数目为3 NA |
| C、标准状况下,11.2 L CCl4所含分子数为0.5 NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标况下,戊烷为液态;
B、根据n=
并结合乙炔的电子式来分析;
C、标况下,CCl4为液态;
D、根据乙烯、丙烯、丁烯的最简式均为CH2来计算.
B、根据n=
| m |
| M |
C、标况下,CCl4为液态;
D、根据乙烯、丙烯、丁烯的最简式均为CH2来计算.
解答:
解:A、标况下,戊烷为液态,故A错误;
B、根据n=
可知26g乙炔的物质的量n=
=1mol,而根据乙炔的电子式可知:1mol乙炔含5mol共用电子对即5NA个,故B错误;
C、标况下,CCl4为液态,故C错误;
D、根据乙烯、丙烯、丁烯的最简式均为CH2可知:14g的混合气体中CH2的物质的量n=
=
=1mol,故含有的原子的物质的量为3mol,个数为3NA个,故D正确.
故选D.
B、根据n=
| m |
| M |
| 26g |
| 26g/mol |
C、标况下,CCl4为液态,故C错误;
D、根据乙烯、丙烯、丁烯的最简式均为CH2可知:14g的混合气体中CH2的物质的量n=
| m |
| M |
| 14g |
| 14g/mol |
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的运用和物质的结构和状态是解题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
采用下列装置和操作,能达到实验目的是( )
A、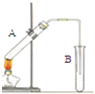 A中为乙醇、醋酸,B中为饱和碳酸钠溶液,制取乙酸乙酯 |
B、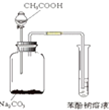 验证醋酸、碳酸、苯酚的酸性强弱 |
C、 用浓硫酸、乙醇共热到约170℃制乙烯 |
D、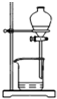 用NaOH溶液除去苯中混有的少量苯酚 |
将0.1molN2O4置于密闭烧瓶中,把烧瓶放入100℃的恒温水浴,烧瓶内气体逐渐变为红棕色:N2O4(g)?2NO2 (g),能说明反应在该条件下达到平衡状态的是( )
| A、N2O4的消耗速率与NO2的生成速率相等 |
| B、烧瓶内气体的颜色不再变化 |
| C、烧瓶内混合气体的质量不再变化 |
| D、烧瓶内混合气体的压强不再变化 |
下列有关物质的性质和该性质的应用均正确的是( )
| A、铝的熔点很高,可用于制作耐高温材料 |
| B、浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体 |
| C、油脂能在酸性溶液中水解生成高级脂肪酸,可用于防止油脂变质 |
| D、过氧化钠能与二氧化碳反应产生氧气,可用于高空飞行或潜水的供氧剂 |
下列各组物理量中,随取水量的变化而变化的是( )
| A、水的沸点 |
| B、水的密度 |
| C、水的物质的量 |
| D、水的摩尔质量 |
全钒液流储能电池(VRB)广泛应用于风能、太阳能发电系统的储能系统.电池反应为VO2++V2++2H+
VO2+V3+H2O,下列说法正确的是( )
| 放电 |
| 通电 |
| A、充电时,外接电源的正极与电池上标注“-”的电极连接 |
| B、电池工作时,H+由正极流向负极 |
| C、电池放电时,负极的电极反应为VO2++H2O=VO2++2H++e- |
| D、电池充电时,阴极的电极反应为V3++e-=V2+ |
下列说法或表示法正确的是( )
| A、由C(s,石墨)→C(s,金刚石)△H=+1.9kJ?mol-1可知,石墨比金刚石稳定 |
| B、在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(1)△H=-285.8kJ?mol-1 |
| C、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| D、压缩容器的体积,平衡2SO2+O2?2SO3正向移动,该反应的△H减小 |