题目内容
11.下列各组中,互称为同分异构体的是( )| A. | O2与O3 | B. | 35Cl与37Cl | C. | CH3CHO与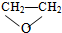 | D. | CH4与C2H6 |
分析 A.由同一种元素组成的不同单质互为同素异形体;
B.同一种元素的不同核素之间互为同位素;
C.分子式相同,结构不同的化合物,互为同分异构体;
D.碳原子数不同的烷烃之间互为同系物.
解答 解:A.O2与O3都是由氧元素组成的不同单质,互为同素异形体,故A错误;
B.35Cl与37Cl都是氯元素的不同核素,互为同位素,故B错误;
C.CH3CHO与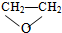 分子式相同,结构不同,互为同分异构体,故C正确;
分子式相同,结构不同,互为同分异构体,故C正确;
D.CH4与C2H6都属于烷烃,互为同系物,故D错误;
故选C.
点评 本题考查了同分异构体的判断,为高频考点,难度不大,注意同分异构体、同素异形体、同位素、同系物的区别.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
1.下列性质中,不能说明乙酸是弱电解质的是( )
| A. | 醋酸钠溶液的PH 大于7 | |
| B. | 常温时,0.1mol/L乙酸溶液的PH约为3 | |
| C. | 乙酸能和碳酸钙反应放出CO2 | |
| D. | PH=1的醋酸溶液用水稀释1000倍后,pH<4 |
2.已知反应:C(s)+CO2(g)?2CO(g)△H>0一定条件下,改变某一个反应条件一定能使反应速率显著加快的是( )
| A. | 降低反应体系的压强 | B. | 增加反应物碳的用量 | ||
| C. | 缩小反应体系的体积 | D. | 减少体系中CO的量 |
19.某温度下,0.200mol•L-1的HA溶液与0.200mol•L-1的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下表,下列说法正确的是( )
| 微粒 | X | Y | Na+ | A- |
| 浓度/(mol•L-1) | 8.00×10-4 | 2.50×10-10 | 0.100 | 9.92×10-2 |
| A. | 0.1mol•L-1HA溶液的pH=1 | B. | 该温度下Kw=1.0×10-14 | ||
| C. | 微粒X表示OH-,Y表示H+ | D. | 混合溶液中:n(A-)+n(X)=n(Na+) |
6.下列仪器及其名称不正确的是( )
| A. |  量筒 | B. |  试管 | C. | 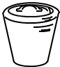 蒸发皿 | D. |  分液漏斗 |
16.在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)?H2(g)+I2(g),2s时生成0.1mol H2,则以HI表示该时段的化学反应速率是( )
| A. | 0.05 mol•Lˉ1•sˉ1 | B. | 0.1 mol•Lˉ1•sˉ1 | ||
| C. | 0.2 mol•Lˉ1•sˉ1 | D. | 0.8 mol•Lˉ1•sˉ1 |
3.下列有关金属的说法中,正确的是( )
| A. | 钠在空气中燃烧只生成白色的氧化钠固体 | |
| B. | 燃着的镁条伸入盛满二氧化碳的集气瓶中不能继续燃烧 | |
| C. | 铜能与氯化铁溶液反应,该反应可以用于印刷电路板的制作 | |
| D. | 铁能与硫酸发生反应,故不能用铁制容器贮存浓硫酸 |
18.下列说法正确的是( )
| A. | 以极性键结合起来的分子一定是极性分子 | |
| B. | 非极性分子中,一定含有非极性共价键 | |
| C. | 乙醇分子和水分子间只存在范德华力 | |
| D. | 卤素单质按F2→I2,熔沸点逐渐升高 |
 .
.