题目内容
2.已知反应:C(s)+CO2(g)?2CO(g)△H>0一定条件下,改变某一个反应条件一定能使反应速率显著加快的是( )| A. | 降低反应体系的压强 | B. | 增加反应物碳的用量 | ||
| C. | 缩小反应体系的体积 | D. | 减少体系中CO的量 |
分析 增加反应速率,则升高温度、增大浓度或增大压强等,注意C为固体的特点,以此解答.
解答 解:A、降低反应体系的压强,反应速率减慢,故A错误;
B、由于碳为固体,增加反应物C的用量,对反应速率没有影响,故B错误;
C、缩小反应体系的体积,压强增大,气体浓度增大,反应速率增大,故C正确;
D、减少体系中CO的量,反应速率减小,故D错误;故选:C.
点评 本题考查化学反应速率的影响,侧重于基础知识的考查,注意相关基础知识的学习,难度不大.

练习册系列答案
相关题目
13.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 2L0.5mol/L亚硫酸钠溶液中含有的H+离子数为2NA | |
| B. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
10.在反应C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O中,氧化剂是( )
| A. | C | B. | HNO3 | C. | CO2 | D. | SO2 |
17.下列各组中的两组物质互为同系物的是( )
| A. | 乙苯与二甲苯 | B. | 乙醇与乙二醇 | C. | 乙烯与聚乙烯 | D. | 甲烷与新戊烷 |
7.某氢氧固体酸燃料电池的总反应为:2H2+O2=2H2O,其基本结构如图所示:
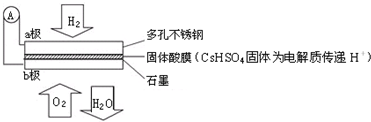
下列有关说法不正确的是( )

下列有关说法不正确的是( )
| A. | 电子通过外电路从a极流向b极 | |
| B. | H+由a极通过固体酸电解质传递到b极 | |
| C. | 电池工作时每转移0.1 mol电子,消耗1.12 LH2 | |
| D. | b极上的电极反应式为:O2+4H++4e-=2H2O |
14.某有机物由C、H、O三种元素组成,分子球棍模型如图所示.关于该有机物叙述正确的是( )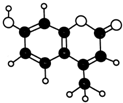

| A. | 分子式为C11H9O3 | B. | 不能使溴水褪色 | ||
| C. | 属于芳香族化合物 | D. | 不能与Na0H溶液反应 |
11.下列各组中,互称为同分异构体的是( )
| A. | O2与O3 | B. | 35Cl与37Cl | C. | CH3CHO与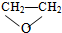 | D. | CH4与C2H6 |
9.阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如图1:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如图1:

主要试剂和产品的物理常数
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是防止乙酸酐水解;
(2)写出制备阿司匹林的化学方程式 ;
;
(3)①合成阿斯匹林时,最合适的加热方法是水浴加热;
②过滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是关闭水龙头,向漏斗中加冰水至浸没沉淀物,使洗涤剂缓慢通过沉淀物,重复上述操作2-3次;
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再过滤,则加饱和NaHCO3溶液的目的是使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,便于与聚合物分离;
另一种改进的提纯方法,称为重结晶提纯法.方法如下:
[粗产品]$→_{沸石}^{乙酸乙酯}$ $→_{回流}^{加热}$ $\stackrel{趁热过滤}{→}$ $→_{抽滤}^{冷却}$ $→_{干燥}^{洗涤}$[乙酰水杨酸]
(5)改进的提纯方法中加热回流的装置如2图所示,使用温度计的目的是控制反应温度,防止温度过高,避免乙酰水杨酸受热分解;冷凝水的流进方向是b(填“b”或“c”)
(6)检验产品中是否含有水杨酸的试剂是FeCl3溶液;
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品m=2.2g,则所得乙酰水杨酸的产率为84.3%.
 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如图1:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如图1:
主要试剂和产品的物理常数
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸 | 102 | 139.4(沸点) | 反应 |
| 乙酸水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是防止乙酸酐水解;
(2)写出制备阿司匹林的化学方程式
 ;
;(3)①合成阿斯匹林时,最合适的加热方法是水浴加热;
②过滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是关闭水龙头,向漏斗中加冰水至浸没沉淀物,使洗涤剂缓慢通过沉淀物,重复上述操作2-3次;
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再过滤,则加饱和NaHCO3溶液的目的是使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,便于与聚合物分离;
另一种改进的提纯方法,称为重结晶提纯法.方法如下:
[粗产品]$→_{沸石}^{乙酸乙酯}$ $→_{回流}^{加热}$ $\stackrel{趁热过滤}{→}$ $→_{抽滤}^{冷却}$ $→_{干燥}^{洗涤}$[乙酰水杨酸]
(5)改进的提纯方法中加热回流的装置如2图所示,使用温度计的目的是控制反应温度,防止温度过高,避免乙酰水杨酸受热分解;冷凝水的流进方向是b(填“b”或“c”)
(6)检验产品中是否含有水杨酸的试剂是FeCl3溶液;
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品m=2.2g,则所得乙酰水杨酸的产率为84.3%.