题目内容
14.液化气的主要成分是丙烷,下列有关丙烷的叙述不正确的是( )| A. | 是直链烃,但分子中3个碳原子不在一条直线上 | |
| B. | 在光照条件下能够与氯气发生取代反应 | |
| C. | 丙烷比丁烷沸点高 | |
| D. | 1 mol丙烷完全燃烧消耗5 mol O2 |
分析 A.烷烃分子中有多个碳原子应呈锯齿形,丙烷中3个C呈V形;
B.丙烷等烷烃在光照的条件下可以和氯气发生取代反应;
C.烷烃中碳个数越多沸点越高;
D.根据丙烷燃烧方程式C3H8+5O2$\stackrel{点燃}{→}$3CO2+4H2O来计算.
解答 解:A.烷烃分子中有多个碳原子应呈锯齿形,丙烷中3个C呈V形,3个碳原子不在一条直线上,故A正确;
B.丙烷等烷烃在光照的条件下可以和氯气发生取代反应,生成氯代烷和HCl,故B正确;
C.烷烃中碳个数越多沸点越高,丙烷分子中碳原子数小于丁烷,故丁烷沸点高,更易液化,故C错误;
D.由丙烷燃烧方程式C3H8+5O2$\stackrel{点燃}{→}$3CO2+4H2O可知,1 mol丙烷完全燃烧消耗5 mol O2,故D正确;
故选C.
点评 本题主要考查烷的结构与性质等,题目难度较小,注意基础知识的积累,把握烷烃的取代反应和燃烧反应是解题的关键,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列反应过程中的能量变化与如图相符的是( )


| A. | 金属钠和水反应 | B. | 生石灰变成熟石灰的反应 | ||
| C. | Al和Fe2O3的铝热反应 | D. | CaCO3受热分解 |
2.下列说法不正确的是( )
| A. | 12C与14C为不同核素 | B. | 石墨和C60互为同素异形体 | ||
| C. | O2和O3互为同位素 | D. | ${\;}_{17}^{35}$X与${\;}_{17}^{37}$Y 为同种元素 |
9.对下列实验现象的原因分析不正确的一项是( )
| 选项 | 实验现象 | 原因分析 |
| A | 久置的浓硝酸呈黄色 | 浓硝酸不稳定,分解生成的NO2 溶解在其中 |
| B | 铝片先用砂纸打磨,再加入到浓硝酸中,无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| C | SO2通入酸性高锰酸钾溶液中,溶液紫红色褪去 | SO2具有漂白性,使其褪色 |
| D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有关化学用语表示正确的是( )
| A. | Mg原子的结构示意图: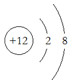 | B. | OCl2分子的电子式: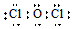 | ||
| C. | HF分子的电子式: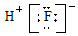 | D. | Na2S形成的电子式 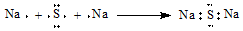 |
6.如图为冰的一种骨架形式,依此为单位向空间延伸,请问该冰中的每个水分子有几个氢键( )


| A. | 2 | B. | 4 | C. | 8 | D. | 1 |
3.在N2+3H2?2NH3的可逆反应中,自反应开始至2s末,氨的浓度由0变为0.8 mol•L-1 则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
| A. | 0.3 mol•L-1•S-1 | B. | 0.4 mol•L-1•S-1 | C. | 0.6mol•L-1•S-1 | D. | 0.8 mol•L-1•S-1 |
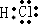 ,X2Y的结构式
,X2Y的结构式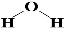 .
.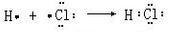 .
.